شیمی اول دبیرستان

| عنوان | پاسخ | بازدید | توسط |
| |
1 | 130 | alireza663 |
| |
8 | 5011 | mina |
| |
0 | 2432 | alex |
| |
0 | 2808 | alex |
| |
0 | 1292 | hesam |
| |
0 | 1546 | hesam |
| |
0 | 1279 | hesam |
| |
0 | 2342 | hesam |
| |
0 | 1286 | hesam |
| |
0 | 1549 | hesam |
شیمی اول دبیرستان
بسم الله النور
اورانیم(Uranium)/نیما حاجیان/کلاس06/دبیرستان ملاصدرا1 اورانیم یکی از عنصرهای شیمیایی است که عدد اتمی آن ۹۲ و نشانه آن U است و در جدول تناوبی جزو آکتنیدها قرار میگیرد. ایزوتوپ ۲۳۵U اورانیم در نیروگاههای انرژی هستهای به عنوان سوخت و در سلاحهایاتمی به عنوان ماده منفجره استفاده میشود.
اورانیم به طور طبیعی فلزی است سخت، سنگین، نقرهای رنگ و پرتوزا. این فلز کمی نرم تر از فولاد بوده و تقریبآ قابل انعطاف است. اورانیم یکی از چگالترین فلزات پرتوزا است که در طبیعت یافت میشود. چگالی آن ۶۵٪ بیشتر از سرب و کمی کمتر از طلا است.
سالها از اورانیم به عنوان رنگ دهنده لعاب سفال یا برای تهیه رنگهای اولیه در عکاسی استفاده میشد و خاصیت پرتوزایی (رادیواکتیو) آن تا سال ۱۸۶۶ میلادی ناشناخته ماند و قابلیت آن برای استفاده به عنوان منبع انرژی تا اواسط قرن بیستم میلادی مخفی بود.
فراوانی
این عنصر از نظر فراوانی در میان عناصر طبیعی پوسته زمین در رده ۴۸ قراردارد.
اورانیم در طبیعت بصورت اکسید و یا نمکهای مخلوط در مواد معدنی (مانند اورانیت یا کارونیت) یافت میشود. این نوع مواد اغلب از فوران آتشفشانها بوجود میآیند و نسبت وجود آنها در زمین برابر دو در میلیون نسبت به سایر سنگها و مواد کانی است. اورانیم طبیعی شامل ۹۹/۳٪ از ایزوتوپ ۲۳۸U و ۰/۷٪ ۲۳۵U است.
این فلز در بسیاری از قسمتهای دنیا در صخرهها، خاک و حتی اعماق دریا و اقیانوسها وجود دارد. میزان وجود و پراکندگی آن از طلا، نقره یا جیوه بسیار بیشتر است.
در ایران بزرگترین منبع اورانیم مربوط به ساغند اردکان می باشد.

به نام خدا
جزوه شیمی 2
لطفا با رمز داده شده در کلاس وارد شوید.
به نام خالق هستی بخش جهان
موضوع:نانوکامپوزیت ها
گردآورنده:محمّدیوسفی
معلم مربوطه:جناب آقای سلامی
کلاس دوم تجربی
دبیرستان شهیدرجایی 1
دسته بندی، خواص و کاربرد
مقدمه
کامپوزیت ترکیبی است که از لحاظ ماکروسکوپی از چند ماده متمایز ساخته شده باشد، به طوری که این اجزاء به آسانی از یکدیگرقابل تشخیص باشند.
به طور نمونه، یکی از کامپوزیت های آشنا بتن است که از دو جزء سیمان و ماسه ساخته شده است.
برای ایجاد تغییر و بهینه کردن خواص فیزیکی و شیمیایی مواد، آن ها را ترکیب یا کامپوزیت می کنیم. به طور مثال پلی اتیلن (PE) که در ساخت چمن های مصنوعی از آن استفاده می گردد، رنگ پذیر نیست و به همین سبب رنگ این چمن ها اغلب مات است. برای برطرف نمودن این نقص به آن وینیل استات می افزایند تا خواص پلاستیکی، نرمیت و رنگ پذیری آن اصلاح شود. در واقع، هدف از ایجاد کامپوزیت، به دست آوردن ماده ای ترکیبی با خواص مورد انتظار می باشد.
نانوکامپوزیت نیز همان کامپوزیت است که یک یا چند جزء از آن، ابعاد کمتر از 100 نانومتر دارد. نانوکامپوزیت ها از دو فاز تشکیل شده اند. فاز اول یک ساختار بلوری است که در واقع پایه یا ماتریس نانوکامپوزیت محسوب می شود و ممکن است از جنس پلیمر، فلز و یا سرامیک باشد. فاز دوم نیز ذراتی در مقیاس نانومتر می باشند که به عنوان تقویت کننده (مواد پرکننده Filler) به منظور اهداف خاص از قبیل استحکام، مقاومت، هدایت الکتریکی، خواص مغناطیسی و ... در درون فاز اول (ماده پایه) توزیع می شوند.
در بحث نانومواد، نانوکامپوزیت ها از جایگاه ویژه ای برخوردار هستند. حضور ذرات و الیاف در ساختار نانوکامپوزیت ها معمولاً باعث ایجاد استحکام در ماده ی پایه می شود. در واقع هنگامی که ذرات و یا الیاف درون یک ماده ی پایه توزیع شوند، نیروهای اعمال شده به کامپوزیت به طور یکنواختی به ذرات یا الیاف منتقل می شود. با توزیع مواد پرکننده درون ماده پایه خصوصیاتی نظیر استحکام، سختی، خواص تربیولوژیکی و تخلخل تغییر می کند. ماده ی پایه می تواند ذرات را به گونه ای از هم جدا نگه دارد که رشد ترک به تأخیر افتد. به علاوه اجزاء نانوکامپوزیت ها بر اثر برهمکنش سطحی بین ماده ی پایه و مواد پرکننده، از خواص بهتری برخوردار می شوند. نوع و میزان برهمکنش ها نقش مهمی در خواص مختلف نانوکامپوزیت ها همچون حلالیت، خواص نوری، خواص الکتریکی و مکانیکی آن ها دارد.
طبقه بندی نانوکامپوزیت ها
انواع نانوکامپوزیت را می توان بر اساس ماده پایه آن ها به شرح زیر طبقه بندی کرد:
نانوکامپوزیت های پایه پلیمری Polymer matrix nanocomposites (PMNCs)1-
نانوکامپوزیت های پایه سرامیکی Ceramic matrix nanocomposites (CMNCs)2-
نانوکامپوززیت های پایه فلزی Metal matrix nanocomposites (MMNCs)3-
در ادامه به بررسی خواص و کاربرد هر یک از این نانوکامپوزیت ها پرداخته می شود.
نانوکامپوزیت های پایه پلیمری
در بین نانوکامپوزیت ها بیشترین توجه به نانوکامپوزیت های پایه پلیمری معطوف است. یکی از دلایل گسترش نانوکامپوزیت های پلیمری، خواص بی نظیر مکانیکی، شیمیایی و فیزیکی آن است. نانوکامپوزیت های پلیمری عموماً دارای استحکام بالا، وزن کم، پایداری حرارتی بالا، رسانایی الکتریکی بالا و مقاومت شیمیایی بالایی هستند. تقویت پلیمرها با استفاده از مواد آلی و معدنی بسیار مرسوم می باشد. بر خلاف تقویت کننده های مرسوم که در مقیاس میکرون می باشند، در نانوکامپوزیت ها تقویت کننده ها ذراتی در ابعاد نانومتر می باشند. با افزودن درصد کمی از نانوذرات به یک پلیمر خالص، استحکام کششی، استحکام تسلیم و مدول یانگ افزایش چشمگیری می یابد. به عنوان مثال، با افزودن تنها 0.04 درصد حجمی میکا (یک نوع سیلیکات) با ابعاد 50 نانومتر به اپوکسی (Epoxy)، مدول یانگ این ماده 58 درصد افزایش خواهد یافت.
دلیل دوم توسعه نانوکامپوزیت های پایه پلیمری و افزایش تحقیقات در این زمینه، کشف نانولوله های کربنی در سال 1991 میلادی است. استحکام و خواص الکتریکی نانولوله های کربنی به طور قابل ملاحظه ای با نانولایه های گرافیت و دیگر مواد پرکننده تفاوت دارد. نانولوله های کربنی موجب رسانایی و استحکام فوق العاده ای در پلیمرها می شوند به طوری که کاربردهای حیرت انگیزی همچون آسانسور فضایی را برای آن می توان متصور شد. از نظر نظامی نیز فراهم کردن هدایت الکتریکی در پلیمرها فرصت های انقلابی را به وجود خواهد آورد. به عنوان مثال از پوسته های الکتریکی-مغناطیسی گرفته تا کامپوزیت های رسانای گرما و لباس های سربازان آینده
این دسته از کامپوزیت ها به دلیل خواص منحصر به فردی که دارند به طور گسترده ای در صنایع خودرو، هوا-فضا و بسته بندی مواد غذایی گسترش یافته اند. از دیگر کاربردهای نانوکامپوزیت های پلیمری پوشش های مقاوم به سایش، پوشش های مقاوم به خوردگی، پلاستیک های رسانا، حسگرها، آسترهای مقاوم در دمای بالا و غشاهای جداسازی گازها و سیالات نفتی می باشند. به عنوان مثال می توان به نوعی غشاء نانوکامپوزیتی ساخته شده از یک نوع پلیمر و نانولایه های سیلیکا اشاره کرد که توسط محققان دانشگاه کارولینای شمالی ساخته شده است. این غشاء توانایی فوق العاده ای در جداسازی مولکول های آلی از گازها دارد.
نانوکامپوزیت های پایه سرامیکی
به مواد (معمولاً جامد) ی که بخش عمده ی تشکیل دهنده آن ها غیرفلزی و غیرآلی باشد، سرامیک گفته می شود. سرامیک ها خواص بسیار خوبی نظیر مقاومت حرارتی بالا، پایداری شیمیایی خوب و استحکام مکانیکی مناسبی دارند، اما به دلیل پیوندهای یونی و کووالانس موجود در سرامیک ها چقرمگی شکست آن ها پایین است و تغییر شکل پلاستیک این مواد محدود می باشد. به منظور رفع این مشکل با اضافه کردن و جداسازی الیاف و ذرات مناسب، می توان چقرمگی شکست را بالا برد. اگر این تقویت کننده ها ابعاد نانومتری داشته باشند بالاترین چقرمگی شکست به دست می آید.
به طور مثال در شکل1 نانوکامپوزیت نیترید سیلیسیم حاوی نانولوله های کربنی چند دیواره، نشان داده شده است. برای ساخت این نانوکامپوزیت از پرس ایزواستاتیک گرم استفاده می شود. از خواص مکانیکی قابل توجه این نانوکامپوزیت ها می توان به استحکام خمشی و مدول الاستیک قابل توجه آن ها اشاره کرد.
نانوکامپوزیت های پایه فلزی
کامپوزیت های پایه فلزی، کم وزن و سبک بوده و به علت استحکام و سختی بالا کاربردهای وسیعی در صنایع خودرو و هوا-فضا پیدا کرده اند. اما این کاربردها به لحاظ کم بودن قابلیت کشش در این کامپوزیت ها محدود شده است. تبدیل کامپوزیت به نانوکامپوزیت سبب افزایش استحکام و رفع محدودیت های مذکور می شود.
نانوکامپوزیت های پایه فلزی اصولاً مشابه روش های متالوژی پودر تولید می شوند. این نانوکامپوزیت ها کاربردهای متفاوتی دارند خصوصاً نانوکامپوزیت های پایه منیزیم که در سال های اخیر به دلیل چگالی کم، استحکام بالا، مقاومت به خزش بالا و پایداری حرارتی مناسب، گسترش چشمگیری داشته اند. نانوکامپوزیت های پایه منیزیم کاربردهای گسترده ای در صنایع هوایی و خودروسازی دارند.
نانوکامپوزیت و فردا
مهمترین تأثیر نانوکامپوزیت ها در آینده از طریق کاهش وزن خواهد بود. اخیراً کامپوزیت های نانوذره سیلیکاتی به بازار خودروها وارد شده اند. در سال 2001 هم جنرال موتور و هم تویوتا شروع تولید محصول با این مواد را اعلام کردند. مزیت این مواد استحکام و کاهش وزن است که مورد آخر صرفه جویی در سوخت را نیز به همراه خواهد داشت.
علاوه بر این نانوکامپوزیت ها به صنعت بسته بندی مواد غذایی نیز راه یافته اند تا سدی بزرگتر در برابر نفوذ گازها و کاهش فساد باشند. محققان معتقدند که افزودن دو درصد نانوذره رس به بسته بندی، 75 درصد تبادل اکسیژن و دی اکسید کربن را کاهش می دهد که این امر به افزایش طول مدت نگهداری مواد غذایی کمک می کند. در مورد ضدباکتریهایی نظیر نانوذرات نقره، این نانوذرات از رشد عوامل زنده فاسده کننده مواد غذایی مانند باکتریها و قارچ ها جلوگیری می کنند.
خواص تعویق آتشگیری نانوکامپوزیت های حاوی نانوذرات سیلیکا، می تواند به خوبی مصارفی در سرویس خواب، پرده ها و محصولاتی از این دست پیدا کند.
به نام خداوندیکتا
موضوع:شیمی نفت
گردآورنده:محمّدیوسفی
معلم مربوطه:آقای سلامی
کلاس دوم تجربی
دبیرستان شهیدرجایی 1
تاریخچه
این ماده را از قرنها پیش بصورت گاز در آتشکده و یا به فرم قیر (کاده ای که پس از تبخیر مواد فرار یا سبک نفت از آن باقی میماند) میشناختهاند یا بطوری که در کتب مقدس و تاریخی اشاره شده است که در ساختمان برج بابل از قیر استفاده گردیده و کشتی نوح و گهواره موسی نیز به قیر اندوده بوده است. بابلیها از قیر بعنوان ماده قابل احتراق در چراغها و تهیه ساروج جهت غیر قابل نفوذ نمودن سدها و بالاخره جهت استحکام جادهها استفاده میکردهاند.
مدت زمان مدیدی ، مورد استعمال نفت فقط برای مصارف خانگی و یا به عنوان چربکنندهها بود، اما از آغاز قرن شانزدهم میلادی روز به روز موارد استعمال آن رو به افزایش نهاد تا اینکه در سال 1854 دو نفر داروساز وجود یک فراکسیون سبک قابل اشتعال را در روغن زمینی تشخیص دادند و همچنین به کمک تقطیر ، مواد دیگری بدست آوردند که برای ایجاد روشنایی بکار میرفت. بر اساس این کار آزمایشگاهی بود که بعدا دستگاههای عظیم تصفیه نفت طرحریزی و مورد بهره برداری قرار گرفت. صنعت نفت در آتازونی در سال 1859 شروع شد.
تاریخچه استخراج نفت در ایران
صنعت نفت ایران نیز از سال 1908 پس از هفت سال تفحص مکتشفین و کشف نفت در مسجدسلیمان واقع در دامنه جبال زاگرس ، پا به عرصه وجود گذاشت.
نفت خام
امروزه چاههای نفت متعددی در سراسر جهان وجود دارد که از آنها نفت استخراج میکنند و به نفتی که از چاه بیرون کشیده میشود، نفت خام میگویند. نفت خام را تصفیه میکنند، یعنی هیدروکربنهای گوناگونی را که نفت خام از آنها تشکیل شده است از یکدیگر جدا میکنند که به این کار پالایش نفت میگویند و در پالایشگاهها این کار انجام میشود. نفت منبع انرژی و سرچشمه مواد اولیه بسیاری از ترکیبات شیمیایی است و این دور از عوامل اصلی اقتصادی مدرن بشمار میرود. در صنایع جدید از ثروت بیکران و تغییر و تبدیل مواد خام اولیه آن بیاندازه استفاده میشد.
تشکیل نفت
نحوه پیدایش نفت دقیقا تشخیص داده نشده و در این مورد فرضیات گوناگونی پیشنهاد شده است. برخی از این تئوریها ، مربوط به مواد معدنی و بعضی دیگر مربوط به ترکیبات آلی میباشد.
تشکیل نفت از مواد معدنی
اساس این فرضیه بر این است که کربورهای فلزی تشکیل شده در اعماق زمین در اثر تماس با آبهایی که در زمین نفوذ مینماید، ابتدا ایجاد هیدروکربورهای استیلنی با رشته زنجیر کوتاه میکند. سپس هیدروکربورهای حاصل در اثر تراکم و پلیمریزه شدن ایجاد ترکیبات پیچیده و کمپلکس را می نماید که اغلب آنها اشباع شده است.
تشکیل نفت از مواد آلی
بر اساس این فرضیه تشکیل نفت را در اثر تجزیه بدن حیوانات در مجاورت آب و دور از هوا میدانند. زیرا در این شرایط ، قسمت اعظم مواد ازته و گوگردی تخریب و مواد چرب باقیمانده در اثر آب ، هیدرولیز میگردد. اسیدهای چرب حاصله ، تحت اثر فشار و درجه حرارت با از دست دادن عوامل اسیدی تولید هیدروکربورهائی با یک اتم کربن کمتر مینماید.
"انگلر Engler" از تقطیر حیوانات دریائی توانسته است مواد نفتی را تهیه نماید و با توجه به خاصیت "چرخش نوری" مواد نفتی که علت آن وجود گلسترین است (ماده ای که در بدن حیوانات وجود دارد) این فرضیه بیان و مورد تایید شده است. در صورتی که فرضیه های دیگر که مبتنی بر اساس مواد معدنی در تشکیل نفت میباشد، هیچگونه توضیح و دلیل قانع کننده ای در مورد این ویژگی نمیتواند بیان نماید.
همچنین نفت میتواند از تجزیه گیاهان تولید گردد. در این حالت ، خاصیت چرخش نور را به علت وجود ترکیب مشابه گلسترین یعنی پلی استرولها میدانند."مرازک Mrazec" ، میکروبها را در این تغییر و تبدیل موثر میداند.
تئوری تشکیل نفت بر مبنای مواد آلی ، فعلا بیشتر مورد قبول میباشد و اختلاف قابل ملاحظهای را که بین ژیزمانها (منابع نفتی) مشاهده میگردد، بعلت شرایط و عوامل مختلف تشیکل ژیزمانها میدانند.
مواد سازنده نفت خام
مواد سازنده نفت از نظر نوع هیدروکربور و همچنین از نظر نوع ترکیبات هترواتم دار بستگی به محل و شرایط تشکیل آن دارد. بنابراین مقدار درصد مواد سازنده نفت خام در یک منبع نسبت به منبع دیگر تغییر میکند. بطور کلی مواد سازنده نفت شامل: هیدروکربورها- ترکیبات اکسیژنه - سولفوره - ازته و مواد معدنی میباشد.
خواص نفت خام
گرانی
چگالی نفتهای خام را بیشتر بر حسب درجه A.P.I به جای گرانی ویژه (چگالی نسبی) بیان میکنند. ارتباط بین این دو ، به گونه ای است که افزایش گرانی API با کاهش گرانی ویژه مطابقت میکند. گرانی نفت خام میتواند بین پایینتر از 10API تا بالاتر از 50API قرار بگیرد، ولی گرانی اکثر نفتهای خام در گستره بین 20 تا 45API قرار دارد. گرانی API همواره به نمونه مایع در 60 درجه فارینهایت اشاره دارد.
مقدار گوگرد
مقدار گوگرد و گرانی API دو خاصیتی هستند که بیشترین اثر را به ارزشگذاری نفت خام دارند. مقدار گوگرد بر حسب درصد وزنی گوگرد بیان میشود و بین 0,1 در صد تا 5 درصد تغییر میکند. نفتهایی که بیش از 0,5 درصد گوگرد دارند، در مقایسه با نفتهای کمگوگردتر ، معمولا محتاج فراورشهای گستردهتری هستند.
نقطه ریزش
نقطه ریزش نفت خام بر حسب F˚ یا c˚ معرف تقریبی پارافینی بودن یا آروماتیکی بودن نسبی آن است. هرچه نقطه ریزش پایینتر باشد، مقدار پارافین کمتر و مقدار آروماتیک بیشتر است.
حلالیت
قابلیت انحلال هیدروکربورها در آب عموما خیلی کم میباشد. مقدار آب موجود در هیدروکربورها با افزایش درجه حرارت زیاد میشود. حلالیت هیدروکربورها در کلروفرم ، سولفورکربن و تتراکلریدکربن حائز اهمیت است که با افزایش درجه حرارت ، زیاد و با افزایش وزن مولکولی کاسته میگردد. قابلیت انحلال آروماتیکها بیشتر بوده و بعد از آنها اولفینها - نفتنها - متانیها قرار دارد.
ضمنا قابلیت انحلال ترکیبات اکسیژنه - ازته - سولفوره ، کمتر از هیدروکربورها میباشد. بالاخره نفت ، حلال هیدروکربورهای گازیشکل و تقریبا تمام هیدرورکربورهای جامد - گریسها - رزینها - گوگرد و ید میباشد.
نقطه جوش
نقطه جوش هیدروکربورهای خالص با وزن مولکولی و همچنین برای سریهای مختلف با تعداد مساوی اتم کربن بترتیب از هیدروکربورهای اشباعشده به اولفینها - نفتنها و آروماتیکها افزایش مییابد. بدین ترتیب نقطه جوش هیدروکربورهای اشباع شده و اولفینها از همه کمتر و سیکلوآلکانها و آروماتیکها از سایرین بیشتر میباشد.
برای برشهای نفتی که مخلوطی از هیدروکربورهای مختلف میباشند، یک نقطه جوش ابتدائی و یک نقطه جوش انتهایی در نظر گرفته میشود و حد فاصل بین این دو نقطه برای یک برش به نوع مواد سازنده اغلب زیاد و متغیر میباشد که به این حد فاصل بین دو نقطه "گستره تقطیر" گفته میشود.
گرمای نهان تبخیر
گرمای نهان تبخیر در یک سری همولوگ از هیدروکربنها بترتیب از مواد سبک به سنگین کاهش مییابد و همچنین مقدار آن از یک سری به سری دیگر ، مثلا بترتیب از آروماتیکها به نفتنها و هیدروکربورهای اشباع شده نقصان مییابد. بنابراین گرمای نهان تبخیر با دانسیته فراکسیون مربوط بستگی دارد.
قدرت حرارتی
قدرت حرارتی عبارت از مقدار کالری است که از سوختن یک گرم ماده حاصل میشود. قدرت حرارتی هیدروکربورها به ساختمان مولکولی آنها و قدرت حرارتی یک برش نفتی به نوع و مواد سازنده آن سبتگی دارد. قدرت حرارتی متان بیشتر از سایر هیدروکربورها و برابر با 13310 کیلوکالری به ازای یک کیلوگرم میباشد و مواد سنگین حاصله از نفت خام دارای قدرت حرارتی در حدود 10000 کیلو کالری میباشد.
اثر اسید نیتریک
هیدروکربورها در اثر اسید نیتریک به ترکیبات نیتره یا پلینیتره تبدیل میشود. نیتراسیون برخی از مواد نفتی منجر به تهیه ترکیبات منفجره یا مواد رنگین میگردد.
موارد استعمال برخی از برش های نفتی بدست آمده از نفت خام:
شیرین کردن آب دریا
یکی از موارد استعمال گازهای نفتی در صنایع وابسته به پالایشگاهها تهیه آب شیرین از آب شور میباشد.
به عنوان سوخت
از جمله ، بنزین برای سوخت موتورهای مختلف ، کروزون سوخت اغلب تراکتورها و ماشینهای مورد استفاده در کشاورزی و همچنین موتورهای جت هواپیماها اغلب از کروزون یا نفت سفید میباشد، گازوئیل که موتورهای دیزل بعنوان سوخت از نفت گاز (گازوئیل) استفاده مینمایند، نفت کوره یا مازوت یک جسم قابل احتراق با قدرت حرارتی 10500 کالری بوده که بخوبی میتواند جانشین زغال سنگ گردد و سوختن آن تقریبا بدون دود انجام میگیرد.
روشنایی
از کروزون جهت روشنایی و همچنین برای علامت دادن به کمک آتش استفاده میشود، چون نقطه اشتعال کروزون بالاتر از 35 درجه است، لذا از نظر آتشسوزی خطری ندارد.
حلال
از هیدروکربورهای C4 تا C10 میتوان برشهائی با دانسیته و نقاط جوش ابتدائی و انتهایی متفاوت تهیه نمود که مورد استعمال آنها اغلب بعنوان حلال میباشد. بعنوان مثال ، اتر نفت یک حلال سبک با نقطه جوش 75-30 درجه سانتیگراد و وایت اسپیریت (حلال سنگین) که از تقطیر بنزین بدست میآید بعنوان حلال ، رنگهای نقاشی و ورنی ها استفاده میگردد. همچنین برای تمیز کردن الیاف گیاهی و حیوانی و یا سطح فلزات از برشهای خیلی فرار (تقطیر شده قبل از 110 درجه سانتیگراد) استفاده میشود.
روان کاری
روغنهای چرب کننده: نوعی روغن که جهت روان کاری بکار میرود. بستگی به شارژ ، سرعت ، درجه حرارت دستگاه دارد.
انواع روغنها عبارتند از:
1.روغن دوک برای چرب کردن دوک ، موتورهای الکتریکی کوچک و ماشین های نساجی و سانتریفوژهای کوچک.
2.روغن ماشینهای یخ سازی جهت روغنکاری کمپرسورهای آمونیاکی کارخانجات یخسازی.
3.روغن ماشینهای سبک جهت روان کاری موتورهای الکتریکی ، دینامها و سانتریفوژهای با قدرت متوسط.
4.روغن ماشینهای سنگین مخصوص روغنکاری موتورهای دیزلی است مانند دیزلهای سورشارژه و غیره
5.روغن برای سیلندرهای ماشین بخار
6.روغن برای توربین ها
روغن برای موتورهای انفجاری( اتومبیل و غیره..).7
8.روغن دنده
9.روغن موتورهایی که دائما با آب در تماس است
گریس ها: یک روان کننده نیمه جامد است و متشکل از یک روغن نفتی و یک پر کننده (از سری صابونهای فلزی) یا سفتکننده (از مواد پلیمری) میباشد. کاربرد گریس بیشتر برای اتومبیلها و برخی صنایع مناسب میباشد.
آسفالت و قیراندودی: در حال حاضر 75 درصد از باقیمانده حاصل از عمل تقطیر در خلاء برای پوشش جادهها مورد استفاده قرار میگیرد.
موارد استعمال داروئی: از قبیل وازلین باعث نرم شدن پوست بدن گردیده و برای بهبود سرمازدگی نیز موثر است.
پارافین: از پارافین ذوب شده و خالص شده جهت ساخت داروهای زیبائی استفاده میگردد.
گلیسیرین: مقدار قابل ملاحظه ای از این ماده ، از نفت تهیه میگردد. علاوه بر مصارفی که گلیسیرین در صنعت (برای تهیه باروت دینامیت ، مرکب و غیره) دارد، از آن برای فرم نگه داشتن پوست بدن و یا تهیه داروهائی از قبیل گلیسیرین یده استفاده میشود.
به نام ایزدمنان
موضوع:رنگها
گردآورنده:محمّدیوسفی
معلم مربوطه:آقای سلامی
کلاس دوم تجربی
دبیرستان شهیدرجایی1
رنگها
رنگ یک ماده مهندسی میباشد، اما برخلاف بعضی از مواد مهندسی یک ماده ساده نیست، یا حتی نمی توان آن را به سادگی به صورت دسته ای از مواد تعریف کرد. رنگ می تواند از هزاران ماده شیمیایی طبیعی و مصنوعی آلی و معدنی تشکیل شود. تهیه فیلمهائی از رنگ که تاثیرات مطلوب را به همراه داشته باشند مستلزم به کارگیری استادانه انواع بسیاری از تکنیکهای مهم با استفاده از مواد اولیه می باشد
بدون شک هرگاه شخصی مواد خامی را که امروزه تهیه کنندگان پوششهای آلی مورد استفاده قرار می دهند با مواد مصرفی 40 سال قبل مقایسه کند از افزایش تعداد وانواع آنها متحیرخواهد شد.
درحقیقت تعداد بی شماری رزین مصنوعی، روغن و رقیق کننده با انواع وسیعی از رنگدانه های معدنی و آلی وجود دارند که می توان در ساخت یک پوشش آلی از آنها استفاده کرد. بنابراین، می توان گفت که ساده ترین پوشش ساخته شده در حقیقت یک سیستم پیچیده است.
یک رنگ برای مصرف کننده نهائی باید دارای خصوصیاتی از قبیل سهولت استعمال، خشک شدن سریع و عدم سینه دادن، ته نشین شدن، جداشدن رنگدانه ها، ژل شدن، پوسته زدن و در نهایت پایداری هنگام نگهداری را دارا باشد. افزودن مقدار کمی از ترکیباتی به غیر از ترکیبات معمولی و اصلی رنگ، برای دستیابی به خواص عملی مطلوب، به دورانهای اولیه صنعت برمیگردد. در طول دوران صنعت تاکنون ترکیباتی از قبیل صابونها، چسبها،سفیده تخم مرغ، صمغهای طبیعی و نوعی از آسفالت به نام گیلسونت همواره برای این منظور مورد استفاده قرار می گرفته است. امروزه، با وجود این که هنوز تعدادی از این مواد مورد استفاده قرار می گیرند، اما مصرف مواد اضافه شونده مصنوعی رو به افزایش نهاده است. در یک عبارت کلی، هر یک از اجزای سازنده رنگ، در حقیقت، یک ماده اضافه شونده است. سازنده های رنگ به دو دسته تقسیم می شوند: قسمت اول شامل آن دسته از مواد میباشد که برای یک رنگ اساسی هستند و قسمت دوم شامل موادی که به منظور بهبود و اصلاح طبیعت و کیفیت رنگ، سهولت روشهای استعمال آن، یا بعضی هدفهای دیگر مورد استفاده قرار می گیرند.
یک رنگ متشکل از رنگدانه، رزین، حلال، خشک کن یا ماده سخت کننده میباشد. با وجود این، هیچ لزومی ندارد که همواره تمام این مواد در یک رنگ وجود داشته باشند. برعکس در اغلب رنگها، مواد اولیه فوق برای به وجود آوردن یک ماده پوشش دهنده نهائی به تنهائی کافی به نظر نمی رسند. اما به هر حال این مواد جزء مواد اصلی رنگ به شمار می روند.
یک فرمول کننده رنگ می تواند از مواد اضافه شونده به عنوان ابزار اساسی برای اصلاح و بهبود پوششها استفاده کند. در صورت استفاده صحیح از مواد اضافه شونده فرمول کننده رنگ می تواند، بدون هیچگونه افزایش در قیمت رنگ، و یا حتی با کاهش دادن آن بدون کاهش کیفیت، رنگی با بالاترین کیفیت را تولید نماید. بنابراین، مواد اضافه شونده یک جزء لازم از پوششها را تشکیل می دهند.
مواد اضافه شونده در رنگ ها
انواع مواد اضافه شونده به رنگ ها که استفاده قرار می گیرند، عبارتند از:خشک کن ها ، مواد ضد پوسته، مواد تعدیل کننده گرانروی و مواد ضد رسوب، ضد سینه دادن، مواد پخش کننده، موادی که کمک به همتراز شدن سطح فیلم رنگ می کنند ، مواد بازدارنده خوردگی ، مواد ضد کپک یا باکتری ، مواد ضد خزه یا ضد جلبک ، موتد ضد کف یا کف زدا ، مواد ضد یخ ، مواد جاذب نور فرابنفش ، مواد کند کننده آتش سوزی ، مواد خوشبو کننده و بو زدا ، مواد مقاوم کننده فیلم رنگ در مقابل رطوبت ، موادی که باعث افزایش نقش چکشی رنگهای چکشی می شوند ، مواد کنترل کننده برق فیلم رنگ (مواد مات کننده) و مواد نرم کننده.
خشک کنها
به طور کلی زمانی که فیلم یک رنگ خشک می شود مراحل زیر اتفاق می افتد:
1-تبخیر مواد فرار: این عمل به ترتیب باعث می شود که:
مایع رنگ غلیظ شود؛
جدائی فاز صورت گیرد(ژلاتینی شدن یا بلور شدن)؛
فشارهای حاصل از انقباض فیلم موجب فشرده شدن دانسیته فیلم گردد؛
رنگ بر روی شیء پخش گردد و آن را مرطوب سازد تا سطح چسبنده ای بین شیء و رنگ ایجاد شود؛
پوسته فیلم کشیده شده و مولکولهائی که در سطح تماس با هوا واقعند دوباره سازمان دهی شوند؛
رنگدانه ها ته نشین و یا غوطه ور شوند.
2-جذب اکسیژن و سایر گازها از هوا: در بسیاری از موارد در خلال جذب اکسیژن واکنشهائی صورت می گیرد که باعث می شود تعداد نسبتا کمی از مولکولها به منومترهای قابل پلیمر شدن تبدیل گردند.
3-مولکولهای کوچکتر مولکولهای بزرگتر را تشکیل می دهند، و در این میان واکنشهای حلقوی صورت می گیرد.
4-ممکن است جدائی فاز صورت گیرد: که در آن مولکولهای پیچیده نامحلول به صورت ذرات امولسیونی کوچک(یا میکرو ژلها) جدا شده و به شکل کلوئیدی در فاز مایع معلق می شوند. مایع پیوستگی خود را به عنوان یک محیط معلق کننده برای کلوئید حفظ می کند، زیرا هنوز مولکولهائی از ذرات همنوع و غیر همنوع وجود دارند که از نظر مولکولی در یک مخلوط بی نظم قابل مخلوط کردن با یکدیگر میباشند تا یک مایع بی شکل را بوجود آورند.
5-ژلاتینی شدن: که نمایانگر آخرین مرحله خشک شدن فیلم رنگ می باشد و آن را مرحله دگرگونی فاز نیز می نامند. در این مرحله ذرات پراکنده یک شبکه به هم پیوسته را تشکیل می دهند، و به این ترتیب جامد خلل و فرج داری بوجود می آید که در حقیقت بخشی از فیلم خشک شده رنگ میباشد، و مایع باقیمانده در درون فضاهای خالی این جامد جای می گیرد. گاهی اوقات قبل از اینکه تمام حلال تبخیر شده باشد ژلاتینی شدن اتفاق می افتد یا ممکن است این عمل تا زمانی که بخش اعظمی از حلال تبخیر و اکسیداسیون بیشتری انجام شود صورت نگیرد.
در بعضی از انواع پوششهای آلی برای تسریع خشک شدن فیلم رنگ از موادی استفاده می شود که آنها را خشک کن می نامند. خشک کنها را می توان به عنوان کاتالیزورهائی تعریف کرد که وقتی به رنگ افزوده می شوند باعث تسریع در خشک شدن یا سخت شدن فیلم رنگ می گردند. بضی ها خشک کنها را به عنوان«قاصدانی» تعریف کرده اند که مولکولهای اکسیژن هوا را می ربایند و آنها را به مولکولهای روغن خشک شونده یا نیمه خشک شونده به کار رفته در ساختمان مولکولی رنگپایه رنگ می رسانند و همین مراحل دوباره تکرار می شود تا اکسیژن بیشتری به مولکولهای روغن برسد.
ضد پوسته ها
زمانی یک فیلم قابل استفاده و عرضه به بازار خواهد بود که بتواند حداقل فیلمی با شرایط مورد نظر تشکیل داده و در زمان مناسب خشک شود. برای ارائه فرمول یک رنگ زمان، انرژی و تلاش بسیاری صرف می شود تا با تعیین نوع و مقدار صحیح از یک یا چند خشک کننده رنگی با بهترین خواص خشک شوندگی تهیه شود. منظور از بهترین خواص خشک شوندگی در یک رنگ آن است که در هنگام استعمال رنگ بر روی سطح پس از آنکه به صورت فیلم درآمد در زمان مناسب همراه با ایجاد بهترین خصوصیات فیزیکی خشک شود. بنابراین، هرگاه رنگ در زمان و مکانی به غیر از زمان و مکان استعمال آن خشک شود، مورد قبول نخوهد بود و این همان پوسته بستن رنگ، از جمله عیوب مهم آن میباشد.
به طور کلی، پوسته بستن رنگ مربوط به تمایل پلیمر شدن و اکسایش رنگپایه های مصرفی در پوششهای محافظت کننده میباشد که موجب خشک شدن رنگ می گردد. ما می خواهیم که رنگ پس از استعمال بر روی سطح خشک شود. و به همین منظور به آن خشک کن اضافه می کنیم. در بعضی فرمول بندیها نه تنها از این طریق به خشک شدن کلی فیلم رنگ دست می یابیم، بلکه یک خشک شدن سطحی سریع نیز در رنگ ایجاد می شود که موجب تشکیل یک پوسته نازک بر روی سطح رنگ می گردد. اگر بخواهیم برای جلوگیری از پوسته بستن مقدار خشک کن را کم کنیم، تنها زمان خشک شدن را افزایش داده ایم نه اینکه از پوسته بستن جلوگیری کرده باشیم. این مسئله مخصوصا در پوششهای سریع خشک شونده آشکار میباشد. البته لازم به تذکر است که مسئله پوسته بستن رنگ همیشه جزء عیوب رنگ نیست، بلکه در بعضی رنگهای تجارتی که باید پس از خشک شدن، فیلم آنها چین و چروک دار باشد مسئله پوسته بستن از اهمیت به سزائی برخوردار خواهد بود.
می توان گفت که طبیعت اجزای متشکله یک رنگ در کارآئی آن، از جمله پوسته بستن، از اهمیت خاصی برخوردار است. همچنین علاوه بر طبیعت اجزای متشکله رنگ، میزان هر یک از آنها نیز در پیدایش خصوصیات مثبت و منفی رنگ موثر هستند. برای مثال، وقتی که در یک رنگ میزان خشک کنهای مصرفی بیش از حد معمول باشد، موجب شدت پوسته بستن رنگ می گردد. از طرف دیگر وجود حلالهای شدیدا فرار رنگی که درب قوطی آن محکم بسته شده و کاملا به دور از هوا میباشد، امکان تشکیل پوسته را به حداقل کاهش میدهد. البته هرگونه کاهشی در گرانروی سیستم رنگ نیز موجب کاهش تمایل به پوسته بستن می گردد، همانطوریکه هرگونه کاهشی در درصد مواد جامد رنگپایه نیز این کار را انجام میدهد.
از میان عواملی که موجب پوسته بستن رنگ می گردند می توان به موارد زیر اشاره کرد:
1-اکسایش سطح رنگ در ظرف محتوی آن
2-ژل شدن رنگ در اثر کاهش حلال؛
ترکیبی از دو مورد 1 و 2 که موجب به هم خوردن موازنه کلوئیدی رنگ می گردد.
بهترین راه برای جلوگیری از پوسته بستن افزودن مواد ضد اکسایش به رنگ میباشد. این گونه مواد بدون آنکه اثر سوئی بر روی خواص مطلوب رنگ داشته باشند، اثرات زیان بار اکسایش زود هنگام رنگ را خنثی می سازند. بسیاری از چربیها و روغنهای چرب به طور طبیعی حاوی مواد ضد اکسایش می باشند و در نتیجه از نظر پوسته بستن مسئله ای را ایجاد نمی کنند. اما در موادی که مقدار این مواد در حد کافی نباشد باید از مواد افزودنی دیگر استفاده کرد.
در ارزیابی و انتخاب یک ماده ضد پوسته علاوه بر چگونگی عملکرد آن در جلوگیری از پوسته بستن، چندین عامل دیگر نیز در نظر گرفته می شود که عبارتند از:
1-میزان تاثیر آن در کند کردن زمان خشک شدن؛
2-سازگاری با سیستمهای رنگ و جلا؛
3-میزان تاثیر آن در تغییر رنگ یا بد رنگ کردن فیلم خشک شده؛
4-میزان تاثیر آن در تغییر رنگ یا بد رنگ کردن اجزای مایع جلا؛
5-بو
علاوه بر این ، یک ماده ضد پوسته نباید هیچ گونه اثر زیان آوری بر روی گرانروی یا سایر خواص رئولوژیکی رنگ، چه در ابتدا و چه در خلال زمان انبار کردن،داشته باشد. همچنین، ماده ضد پوسته نباید اثر ناخواسته و نامطلوبی بر روی براقیت و دوام کلی فیلم رنگ بگذارد.
کارآئی ضد پوسته های مختلف با نوع رنگپایه ای که ضد پوسته در آن مورد استفاده قرار می گیرد، فرق می کند. مواد ضد پوسته را می توان به سه دسته تقسیم کرد:
1-اکسیم ها
2-پلی هیدروکسی فنلها و مشتقاتش
3-موادی از نوع حلالها که به عنوان یک ماده دیسپرس کننده محصولات شدیدا پلیمری عمل کرده و در نتیجه مانع ژل شدن ذرات می گردند.
مواد تعدیل کننده گرانروی و مواد ضد رسوب:
فرمول بندی رنگ ممکن است موجب تولید رنگهائی شود که بیش از حد سیال و روان باشند. رنگ مایعی که گرانروی آن پائین باشد ممکن است سیالیت آن بیش از حد لزوم برای مقصود نهائی باشد، هر چند سیالیت زیاد در شرایط ممکن است بسیار سودمند هم باشد. بنابراین گرانروی پائین در رنگین کننده ها، بتونه ها و لاکهای اسپری ممکن است مطلوب باشد ولی در پوششهائی که فیلم خشک شده آنها ضخامت بالائی دارد و همچنین رنگهائی که به وسیله قلم مو مصرف می شوند، چنین نمی باشند. در رنگهای با گرانروی پائین، رسوب رنگدانه ها در خلال مدت نگهداری، بخصوص اگر رنگدانه ها بهم فشرده باشند،اتفاق می افتد. این رسوب سنگین ممکن است در دیسپرسیون مجدد نیز اشکالاتی تولید کند. این اشکالات مربوط به روانی و سیالیت و رسوب رنگدانه را می توان با تنظیم گرانروی رنگ از بین برد. به وسیله انتخاب صحیح رنگدانه ها می توان کنترلهای بیشتری برای جلوگیری از رسوب بکار برد
گرانروی رنگ می تواند به وسیله افزودن مواد ضخیم کننده و غلیظ کننده افزایش داده شود، (یعنی سیالیت و روانی رنگ کم شود)، بدون اینکه حالت تیکسوتروپی در رنگ به وجود بیاید. عوامل ایجاد کننده حالت تیکسوتروپی، به رنگ ساختمان ژل مانندی می دهد. این حالت ژل مانند برای بسیاری از رنگهائی که به وسیله قلم مو مصرف می شوند، مفید است زیرا که از سینه دادن و شره کردن آن جلوگیری می نماید. این خاصیت نیز می تواند مسئله رسوب در مدت نگهداری را کاهش داده و یا بطور کلی از بین ببرد.
رنگهائی که حالت تیکسوتروپی دارند در تمام کاربردها مطلوب نیستند، برای مثال وقتی سیالیت خوب مورد نظر است، در این موقع نیز رسوب رنگدانه ها را می توان با مواد ضد رسوب یا فعال کننده سطح مانند سویالستین در حدود 1 درصد فرمول بندی کاهش داد. مواد فعال کننده سطح به سطح رنگدانه جذب می گردد که در نتیجه باعث افزایش حجم و کاهش وزن مخصوص آن می شود. نتیجه نهائی کاهش میزان رسوب است. دیسپرسیون مجدد رنگدانه های رسوب کرده به وسیله استفاده از رنگدانه یارهای فعال شده تسهیل می گردد، که معمولا این رنگدانه یار، کربنات کلسیم به میزان 5 درصد وزن رنگدانه می باشد. ذرات این رنگدانه یارها به دلیل دارا بودن لایه سطح آلی بسیار پرحجم می باشد و در خلال رسوب ذرات بین ذرات رنگدانه مستقر می شوند. وقتی رنگ بهم زده می شود ذرات رنگدانه یار به شکستن تجمع رنگدانه کمک می کند و در نتیجه دیسپرسیون مجدد به راحتی انجام می شود.
بسیاری از مواد، گرانروی رنگ را افزایش می دهند و یا موجب بوجود آمدن حالت تیکسوتروپی در فرمول بندی می گردند. متداولترین انواع این مواد عبارتند از : اترهای سلولز، سیلیکاهای میکرونیزه ، پنتونیتها
مواد ضد کف و کف زدا
کف سیستمی متشکل از دو فاز گاز و مایع می باشد که فاز گاز در فاز مایع پخش شده است. هنگام کار با دستگاههای مخلوط کنی و پر کردن رنگ کف ایجاد می شود و این مسئله موجب کند شدن سرعت تولید، مسدود شدن پمپها و لوله ها و افزایش هزینه تولید رنگ می گردد. لذا، باید در زمان تولید رنگ موادی به آن افزود که بتوان یا مانع ایجاد کف شد و یا اینکه آن را از بین برد. این مواد را تحت عنوان «مواد ضد کف» و یا «مواد کف زدا» می شناسند اما از نظر دسته بندی کلی مواد افزودنی رنگ می توان آنها را جزء «مواد فعال کننده سطح» بشمار آورد.
انتخاب مناسبترین و موثرترین ماده کف زدا یا ضد کف یک مسئله نسبتاً مشکل می باشد، اما، قوانین زیر، هر چند که ثابت نیستند، می توانند کمک زیادی به این امر کنند:
1-کشش سطحی ضد کف باید از کشش سطحی محلول کف کننده کمتر باشد
2-ضد کف باید در محلول کف کننده قابلیت حلالیت پائینی داشته باشد
3-ضد کف باید با محلول کف کننده به آسانی پخش شود
4-ضد کف بایدب ا محلول کننده واکنشی انجام ندهد
5-ضد کف باید ضریب گسترش بالائی داشته باشد
6-ضد کف نباید اثرات زیان آوری در محصول نهائی ایجاد کند
7-در مواردی که داشتن بو یا مزه مهم باشد، ضد کف نباید بو یا مزه خاصی از خود بجای بگذارد
8-ضد کف نباید موجب تجمع رنگدانه و ناپایداری امولسیون شود
9-ضد کف باید با مخلوط کف کننده امتزاج پذیری خوبی داشته باشد تا از پیدایش معایبی از قبیل چشم ماهی شدن یا ژل شدن فیلم خشک نشده رنگ جلوگیری شود
10-ضد کف باید فعالیت خود را برای یک زمان طولانی حفظ کند.
لازم به تذکر استکه علاوه بر عوامل فوق، عوامل دیگری از قبیل گرانروی و سایر اجزای متشکله رنگ، دماف سرعت فرایند تولید نیز در کارائی ماده ضد کف یا کف زدا موثر هستند.
مهمترین مواد ضد کف یا کف زدای مصرفی سیلیکونها، بعضی الکلهای شش الی ده کربنه (مثلا تونیل الکل)، مشتقات پلی اتیلن اکساید و پلی پروپلین اکساید و بعضی از محصولات طبیعی مانند ترپنتین، روغن کاج و روغن پشم و غیره می باشد. از آنجا که خواص ضد کف در فرمول بندیهای گوناگون متفاوت است نوع و مقدار قابل استفاده هر یک از این مواد یکسان نیست. پیشنهاد می شود که برای استفاده از نوع و میزان مصرف هر یک از مواد ضد کف یا کف زدا از توصیه ها و اطلاعات سازندگان آنها کمک گرفته شود. معمولا سازندگان این گونه مواد درصد ماده فعال موجود در آنها را چنان تنظیم می کنند که حدود 1/0 تا 5/0 درصد از کل وزن رنگ را بخود اختصاص دهند.
آب بدلیل کشش سطحی و قطبیت بالا فاز مایع مناسبی برای ایجاد کف بشمار می آید، لذا در ساخت رنگهای امولسیونی استفاده از مواد ضد کف بسیار ضروری و مفید می باشد. رنگهای ساخته شده از رزینهای امولسیون آکریلیک ، پلی وینیل استات ، پلی وینیل الکل ، آلکید و کائوچو نیاز حتمی به اینگونه مواد دارند.
در صنعت رنگسازی تفاوت زیادی بین مواد ضد کف و کف زدا وجود ندارد و هر دو تحت یک عنوان به فروش می رسند. از مواد ضد کف در تولیداتی که هدف جلوگیری از تشکیل کف است استفاده می شود و در صورتی که مواد کف زدا هنگامی استفاده می شوند که منظور از بین بردن کف تولید شده است.
یکی از روشهای عمومی در صنعت رنگسازی این است که نصف مواد ضد کف مورد نظر را ضمن پخش کردن رنگدانه به مخلوط رنگ می افزایند تا از تشکیل کف جلوگیری شود. سپس بقیه مواد ضد کف را در مرحله همرنگ کردن رنگ جهت عدم تشکیل کف بیشتر در هنگام پرکردن قوطیها و استعمال رنگ اضافه می کنند. البته استفاده از دو نوع ماده ضد کف هم منطقی بنظر می آید، زیرا ممکن است یکی از آنها در شرایط سخت پخش رگدانه موثرتر باشد و دیگری در شرایط نگهداری طولانی مدت رنگ مفیدتر واقع شود.
به نام خداوندجان آفرین
موضوع:چسبها,انواع وکاربردآنها
گردآورنده:محمّدیوسفی
معلم مربوطه:جناب آقای سلامی
کلاس دوم تجربی
دبیرستان شهیدرجایی1
چسب
ساخت و مصرف چسب از گذشته رایج بوده است. در قدیم ، از موادی چون قیر و صمغ درختان به عنوان چسب استفاده میکردند. در تمام قرون گذشته و همچنین قرن نوزدهم چسبها منشاء حیوانی و یا گیاهی داشتهاند. چسبهای حیوانی بطور عمده بر مبنای کلوژن مامالیام Mammaliamبودند که پروتئین اصلی پوست ، استخوان و رگ و پی است و چسبهای گیاهی از نشاسته و دکسترین دانههای گندم ، سیب زمینی و برنج تهیه میشدند
کاربردهای متنوع چسب
از قرن نوزدهم بتدریج با پیدایش چسبهای سنتتیک ساخته شده در صنعت پلیمر ، چسبهای سنتی و گیاهی و حیوانی از صحنه خارج شده است. صنعت چسب به صورت گسترده ای در حال رشد میباشد و تعداد محدودی وسایل مدرن ساخت بشر وجود دارد که از چسب در آنها استفاده نشده است. در اتصالات اغلب وسایل از یک جعبه بسیار ساده غلات گرفته تا هواپیمای پیشرفته بوئینگ 747 از چسب استفاده شده است
امکانات بشر میتواند بوسیله چسبها اصلاح گردد. این مطلب ، شامل استفاده از سیمانهای سخت شده توسط UV در دندانپزشکی و سیمانهای پیوند
آکلریلیک در جراحی استخوان میباشد. پیشرفت جدیدی که اخیرا در کاربرد چسب حاصل گشت، اتصال ریلهای فولادی و تراموای جدید شهر منچستر بود. چسبها نه تنها برای موادی که بایستی چسبانده و بهم پیوسته شوند، بلکه در ایجاد چسبندگی برای موادی از قبیل جوهر تحریر ، رنگها و سایر سطوح پوششی ، وسایل بتونه کاری و وجوه میانی در مواد ترکیبی از قبیل فولاد یا بافت پارچه ، در تایرهای لاستیکی و شیشه یا الیاف در پلاستیکها ضروری هستند.
اجزای تشکیل دهنده چسبها
مواد پلیمری
چسبها ، همگی حاوی پلیمر هستند یا پلیمرها در حین سخت شدن چسبها بوسیله واکنش شیمیایی پلیمر شدن افزایشی یا پلیمر شدن تراکمی حاصل میشوند. پلیمرها به چسبها قدرت چسبندگی میدهند. میتوان آنها را به صورت رشتههایی از واحدهای شیمیایی همانند که بوسیله پیوند کووالانسی به هم متصل شدهاند، در نظر گرفت.
پلیمرها در دماهای بالا روان میگردند و در حلالهای مناسب حل میگردند. خاصیت روان شدن آنها در چسبهای حرارتی و خاصیت حل شوندگی آنها در چسبهای بر پایه حلال ، یک امر اساسی میباشد. پلیمرهای شبکهای در صورت گرم شدن جریان نمییابند، ممکن است در حلالها متورم گردند، ولی حل نمیشوند. تمامی چسبهای ساختمانی ، شبکهای هستند، زیرا این مورد خزش (تغییر شکل تحت بار ثابت) از بین میبرد.
افزودنیهای دیگر:
بسیاری از چسبها ، علاوه بر مواد پلیمری دارای افزودنیهایی هستند از قبیل:
مواد پایدار کننده در برابر تخریب توسط اکسیژن و UV
مواد نرم کننده که قابلیت انعظاف را افزایش میدهد و دمای تبدیل شیشهای (Tg ) را کاهش میدهد
مواد پر کننده معدنی که میزان انقباض در سخت شدن را کاهش میدهد و خواص روان شدن را قبل از سخت شدن تغییر میدهد و خواص مکانیکی نهایی را بهبود میبخشد
مواد تغلیظ کننده
معرف های جفت کننده سیلانی
تئوریهای چسبندگی
درباره چسبندگی شش تئوری وجود دارد که عبارتند از:
تئوری جذب فیزیکی
جذب فیزیکی شامل نیروهای واندروالسی در بین سطوح میباشد که در بر گیرنده جاذبههای بین دو قطبیهای دائم و دو قطبی القایی و نیروهای لاندن میباشد.
تئوری جذب شیمیایی
تئوری پیوند شیمیایی در مورد چسبندگی ، بر اساس تشکیل پیوندهای کووالانسی ، یونی و هیدروژنی بین سطح میباشد. مدارکی مبنی بر اینکه پیوندهای کووالانسی با عوامل جفت کنندگی سیلانی تشکیل میشود، وجود دارد و ممکن است که چسبها شامل گروههای هیدروکسی یا آمین باشند که با اتمهای هیدروژن فعال از قبیل گروههای هیدروکسیل ، اگر چوب یا کاغذ اجزا مورد عمل باشند، پیوند هیدروژنی ایجاد میکنند.
تئوری نفوذ
تئوری نفوذ این دیدگاه را مطرح میکند که پلیمرها هنگام تماس ممکن است در همدیگر نفوذ کنند. بنابراین مرز درونی سرانجام برداشته میشود و نفوذ پلیمرها در صورتی اتفاق میافتد که زنجیرهای متحرک و سازگار باشند. به عبارت دیگر ، دما باید از دمای تبدیل شیشهای بالاتر رود.
تئوری الکتروستاتیک
تئوری الکتروستاتیک ، از این طرح سرچشمه گرفته است که وقتی دو فلز در تماس با یکدیگر باشند، الکترونها از یکی به دیگری منتقل میشوند و بنابراین یک لایه مضاعف الکتریکی تشکیل میگردد که نیروی جذب را نشان میدهد. چون پلیمرها ، نارسانا هستند، مشکل به نظر میرسد که این تئوری برای چسبها کاربرد داشته باشد.
تئوری پیوند درونی مکانیکی
اگر سطحی را که میخواهیم روی آن چیزی بچسبانیم، دارای سطحی نامنظم باشد آنگاه ممکن است چسب در ناهمواریهای سطح ، قبل از سخت شدن داخل شود. این ایده ، باعث ظهور این تئوری شد که به اتصالات چسب با مواد متخلخل از قبیل چوب و نسوجات بسط داده شد. مثالی از این قبیل ، عبارت از استفاده از اتو در لایه چسب و در لباس میباشد. لایه چسبها ، حاوی چسبهای ذوبی هستند که پس از ذوب در پارچه نفوذ میکنند..
تئوری لایه مرزی ضعیف
تئوری لایه مرزی ضعیف ، پیشنهاد میکند که سطوح تمیز ، پیوندهای قویتری با چسب ایجاد میکنند. اما برخی آلودگیها از قبیل زنگ و روغن یا گریسها ، لایه ای ایجاد میکنند که چسبندگی ضعیفی دارد. همه آلودگیها ، لایه مرزی ضعیف تشکیل نمیدهند، زیرا در برخی حالات ، آنها توسط چسب حل خواهند شد. در این محدوده ، چسبهای ساختمانی آکریلیک ، برتر از اپوکسیدها هستند و این ، بدلیل توانایی آنها برای حل کردن روغنها و گریسها میباشد.
آماده سازی سطح برای چسبندگی
آماده سازی نامناسب یا نادرست سطح ، احتمالا دلیل عمده شکسته شدن اتصالات چسبی میباشد. آماده سازی سطح یک جسم با روشهای زیر انجام میگیرد: روش های سائیدگی ، استفاده از حلالها ، تخلیه شعله وکرونا ، حک کردن تفلون ، حک کردن فلزات ، آندی کردن فلزات ، استفاده از چند سازه ها
انواع چسبها
چسبهایی که توسط واکنش شیمیایی سخت میشوند:
چسبهای اپوکسیدی:
اپوکسیدها ، بهترین نوع چسبهای شناخته شده ساختمانی هستند و بیشترین کاربرد را دارند. رزین اپوکسی که اغلب در حالت معمول استفاده میشود، معمولا دی گیلیسریل اتراز بیس فنل DGEBA)A) نامیده میشود و بوسیله واکنش نمک سدیم از بیس فنل A با اپی کلروهیدرین ساخته میشود. آمینهای آروماتیک و آلیفاتیک به عنوان عامل سخت کننده استفاده میشوند. این چسبها به چوب ، فلزات ، شیشه ، بتن ، سرامیکها و پلاستیکهای سخت بخوبی میچسبند و در مقابل روغنها ، آب ، اسیدهای رقیق ، بازها و اکثر حلالها مقاوم هستند. بنابراین کاربرد بیشتری در چسباندن کفپوشهای وینیلی در سرویسها و مکانهای خیس و به سطوح فلزی دارند.
چسبهای فنولیک برای فلزات:
وقتی که فنل با مقدار اضافی فرمالدئید تحت شرایط بازی در محلول آبی واکنش کند، محصول که تحت عنوان رزول شناخته شده و الیگومری شامل فنلهای پلدار شده توسط اتروگرومتیلن روی حلقههای بنزن میباشد، بدست میآید. برای جلوگیری از تشکیل حفرههای پر شده از بخار ، اتصالات چسبهای فنولیک تحت فشار ، معمولا بین صفحات پهن فولادی گرم شده توسط پرس هیدرولیک سخت میشوند. بدلیل شکننده بودن فنولیکها ، پلیمرهایی از جمله پلی وینیل فرمال ، پلی وینیل بوتیرال ، اپوکسیدها و لاستیک نیتریل اضافه میشود تا سختتر گردند.
چسبهای تراکمی فرمالدئید برای چوب:
تعدادی از چسبهای مورد استفاده برای چوب نتیجه تراکم فرمالدئید با فنول و رزوسینول (1و3 دی هیدروکسی بنزن) هستند. بقیه با اوره یا ملامین متراکم میشوند.
چسبهای آکریلیک:
چسبهای ساختاری شامل منومرهای آکریلیک توسط افزایشی رادیکال آزاد در دمای محیط سخت میشوند. منومر اصلی ، متیل متاکریلات (MMA) میباشد، اما موارد دیگری از قبیل اسید متاکریلات برای بهبود چسبندگی به فلزات بوسیله تشکیل نمکهای کربوکسیلات و بهبود مقاومت گرمایی و اتیلن گلیکول دی متیل اکریلات برای شبکهای کردن نیز ممکن است مورد استفاده قرار گیرد.
کلروسولفونات پلی اتیلن ، یک عامل سخت کننده لاستیک است و کیومن هیدورپراکساید و N,N دی متیلن آنیلین ، اجزاء یک آغازگر اکسایشی- کاهشی هستند. پیوند دهنده هایی که برای اتصالات محکم مصنوعی به استخوانهای انسان و پوششهای چینی برای دندانها استفاده میشود نیز بر مبنای MMA هستند و بطورکلی برای جسباندن فلزات ، سرامیکها ، بیشتر پلاستیکها و لاستیکها استفاده میشود و اتصالات پرقدرتی را ایجاد میکنند.
چسبهای غیر هوازی:
چسبهای غیر هوازی در غیاب اکسیژن که یک بازدارنده پلیمر شدن است، سخت میگردد. این چسبها اغلب بر پایه دی متاکریلاتهایی از پلی اتیلن گلیکول هستند. کاربرد این چسبها ، اغلب در محل اتصال چرخ دنده ها ، تقویت اتصالات استوانهای و برای دزدگیری میباشد.
چسب های پلی سولفیدی:
پلی سولفیدها در ابتدا به عنوان دزدگیر استفاده میشدند و یک کاربرد مهم دزدگیری لبههای آینههای دوبل میباشد. هر دو برای اینکه واحدها را باهم نگه دارند و مانعی در برابر نفوذ رطوبت ایجاد کنند. آنها به وسیله بیس (2- کلرواتیل فرمال) با سدیم پلی سولفید تهیه میشوند و به منظور کاهش قیمت از پرکننده های معدنی استفاده میشود. به عنوان نرم کننده ، از فتالاتها و معرفهای جفت کننده سیلانی استفاده میشود و عامل سخت کننده آنها شامل دی اکسید منگنز و کرومات هستند.
سفت شدن لاستیکی چسبهای ساختمانی:
بسیاری از چسبهای ساختمانی ، پلیمرهای لاستیکی حل شده ای در خودشان دارند. وقتی که چسبها سخت میشوند، لاستیک به صورت قطراتی با قطر حدود 1µm رسوب میکند. لاستیکهای استفاده شده در این روش شامل پلی وینیل فرمال (pvf) و پلی وینیل بوتیرال (PVB) هستند که هر دو بوسیله واکنش آلدئید مناسب با پلی وینیل الکل ساخته میشوند.
سیلیکونها
چسبهای یک جزئی سیلیکون اغلب به چسبهای ولکانیزه شونده در دمای اطاق (rtv) معروفند و شامل پلی دی متیل سیلوکسان (PDMS) با جرمهای مولکولی در محدود 1600-300 با گروههای انتهای استات ، کتوکسیم یا اتر هستند. این گروهها توسط رطوبت اتمسفر ، هیدرولیز شده ، گروههای هیدروکسیل تشکیل میدهند که بعدا با حذف آب متراکم میشوند.
چسبهای سیلیکونی نرم و مطلوب هستند و دارای مقاومت محیطی و شیمیایی خوبی هستند. این چسبها به عنوان بهترین پوشش برای استفاده در حمام شناخته شدهاند.
چسب چوب
چسبهایی که بدون واکنش شیمیایی سخت میشوند
این چسبها شامل سه نوع زیر میباشند:
چسبهایی که در اثر حذف حلال سخت میشوند.
چسبهای تماسی: چسبهای تماسی احتمالا از معروفترین چسبها بر پایه حلال هستند. اینها محلولهایی از پلیمر در حلال آلی هستند که در دو سطح بکار میروند تا متصل شوند. ماده اصلی این چسبها ، لاستیک پلی کلروپرن (پلی کروپرن ، پلی کلرو بوتادین) است و برای چسباندن روکشهای تزئینی و پلاستیکهای محکم دیگر مثل ABS , DVC به چوپ و محصولات فلزی و چسبهای تماسی DIY برای تخت کفش بکار میروند.
چسبهای پمادی: چسبهای بر پایه حلال مشهور که در ظروف پماد مانند به عموم فروخته میشوند، اغلب محلولهایی از لاستیک نیتریل (همیپلیمر یا بوتادین و آکریلونیتریل) در حلالهای آلی هستند.
چسبهایی که با از دست دادن آب سخت میشوند:
محلولهای آبی و خمیرها: نشاسته ، ذرت و غلات ، منابع عمده برای استفاده چسب هستند. موارد مصرف عمده برای چسباندن کاغذ ، مقوا و منسوجات میباشد. کاربردهای آن شامل صفحات موجدار ، پاکتهای کاغذی ، پنجرگیری تیوپ ، چسباندن کاغذ دیواری و چسبهای تر شدنی مجدد با آب میباشد. چسبهای تر شدنی توسط آب شامل پلی (وینیل الکل) (DVOH) که در تمبرهای پُستی مورد استفاده قرار میگیرند و از لاتکس صمغهای طبیعی (مثلا صمغی و دکسترین) و پلی وینیل استات (DVN) همراه با مقدار زیادی DVOH پایدار کننده تولید میشوند. DVOH تنها پلیمرمعروفی است که از منومر خودش ساخته نمیشود.
به نام خداوندمهربان
موضوع:شیمی محلولها
گردآورنده:محمّدیوسفی
معلم مربوطه:آقای سلامی
کلاس دوم تجربی
دبیرستان شهیدرجایی1
شیمی محلولها
محلولها ، مخلوطهایی همگن هستند. محلولها را معمولا بر حسب حالت فیزیکی آنها طبقه بندی میکنند: محلولهای گازی ، محلولهای مایع و محلولهای جامد.
محلولها ، مخلوطهایی همگن هستند. محلولها را معمولا بر حسب حالت فیزیکی آنها طبقه بندی میکنند محلولهای گازی ، محلولهای مایع و محلولهای جامد. بعضی از آلیاژها محلولهای جامدند؛ سکههای نقرهای محلولهایی از مس و نقرهاند و برنج محلولی جامد از روی در مس است. هر آلیاژی محلول جامد نیست، بعضی از آلیاژها مخلوطهایی ناهمگن اند. محلولهای مایع متداولترین محلولها هستند و بیشترین کاربرد را در بررسیهای شیمیایی دارند. هوا هم مثالی برای محلولهای گازی میباشد.
● ماهیت محلولها
در یک محلول ، معمولا جزئی که از لحاظ کمیت بیشترین مقدار را دارد، حلال و سایر اجزا را مواد حل شده (حل شونده) میگوییم. اما گاهی آسانتر آن است که جزئی از محلول را با آنکه مقدارش کم است، حلال بنامیم و گاهی اصولا اطلاق نام حلال و حل شونده به اجزای یک محلول (مثلا محلولهای گازی) چندان اهمیتی ندارد.
بعضی از مواد به هر نسبت در یکدیگر حل میشوند.امتزاج پذیری کامل از ویژگیهای اجزای تمام محلولهای گازی و بعضی از اجزای محلولهای مایع و جامد است. ولی غالبا، مقدار ماده ای که در حلال معینی حل می شود، محدود است. انحلال پذیری یک ماده در یک حلال مخصوص و در دمای معین، بیشترین مقداری از آن ماده است که در مقدار معینی از آن حلال حل می شود و یک سیستم پایدار به وجود می آورد.
● غلظت محلول
برای یک محلول معین ، مقدار ماده حل شده در واحد حجم حلال یا در واحد حجم محلول را غلظت ماده حل شده میگوییم. مهمترین نوع غلظتها که در آزمایشگاه بکار میرود مولاریته و نرمالیته است.
● انواع محلولها
▪ محلولهای رقیق
محلولهایی که غلظت ماده حل شده آنها نسبتا کم است
▪ محلولهای غلیظ
محلولهایی که غلظت نسبتا زیاد دارند
▪ محلول سیر شده
اگر مقدار ماده حل شده در یک محلول برابر با انحلال پذیری آن در حلال باشد، آن محلول را محلول سیر شده مینامیم. اگر به مقداری از یک حلال مایع ، مقدار زیادی ماده حل شونده (بیشتر از مقدار انحلال پذیری آن) بیفزاییم، بین ماده حل شده و حل شونده باقیمانده تعادل برقرار میشود. ماده حل شونده باقیمانده ممکن است جامد ، مایع یا گاز باشد. در تعادل چنین سیستمی ، سرعت انحلال ماده حل شونده برابر با سرعت خارج شدن ماده حل شده از محلول است. بنابراین در حالت تعادل ، غلظت ماده حل شده مقداری ثابت است.
▪ محلول سیر نشده
غلظت ماده حل شده در یک محلول سیر نشده کمتر از غلظت آن در یک محلول سیر شده است.
▪ محلول فراسیرشده
میتوان از یک ماده حل شونده جامد ، محلول فراسیر شده تهیه کرد که در آن، غلظت ماده حل شده بیشتر از غلظت آن در محلول سیر شده است. این محلول ، حالتی نیم پایدار دارد و اگر مقدار بسیار کمی از ماده حل شونده خالص بدان افزوده شود، مقداری از ماده حل شده که بیش از مقدار لازم برای سیرشدن محلول در آن وجود دارد، رسوب میکند.
● خواص فیزیکی محلولها
بعضی از خواص محلولها به دو عامل ، نوع ماده حل شده و غلظت آن در محلول بستگی دارند. این مطلب برای بسیاری خواص فیزیکی محلولها از جمله ، محلولهای آبی درست به نظر میرسد. برای مثال، محلول نمک طعام در آب بی رنگ پرمنگنات پتاسیم در آب، بنفش صورتی است (در اینجا نوع ماده حل شده مطرح است). افزون بر این ، میدانیم که هر چه بر محلول پرمنگنات آب بریزیم و آن را رقیقتر کنیم، از شدت رنگ آن کاسته میشود (اینجا غلظت محلول مطرح است)
یکی دیگر از خواص فیزیکی که به این دو عامل بستگی دارد، قابلیت هدایت الکتریکی محلول آبی مواد گوناگون است.
چهار خاصه فیزیکی دیگر از محلولها وجود دارد که به نوع و ماهیت ذرات حل شده بستگی ندارد، بلکه فقط به مجموع این ذرات وابسته است. به عبارت دیگر ، تنها عامل موثر بر خواص محلول در اینجا ، غلظت است. چنین خواصی از محلول را معمولا "خواص جمعی محلولها" (خواص کولیگاتیو)).Colligative properties) مینامند
و عبارتند از کاهش فشار بخار ، صعود نقطه جوش ، نزول نقطه انجماد و فشار اسمزی.
▪ کاهش فشار بخار
وقتی یک حل شونده غیر فرار در یک حلال حل میشود، فشار بخار آن کاهش مییابد و مقدار کاهش به مقدار حل شونده بستگی دارد. هر چه میزان حل شونده بیشتر باشد، میزان کاهش در فشار بخار بیشتر است. برای مثال اگر دو ظرف را در نظر بگیریم که در آنها مقدار مساوی مایع وجود دارد که یکی محتوی مولکولهای آب خالص و دیگری محتوی محلول قند در آب است، بدیهی است که تعداد مولکولهای آب در واحد حجم از آب قند ، کمتر از آب خالص است. به همین نسبت ، تعداد مولکولهای آب در سطح آب قند ، نیز کمتر میباشد. بنابراین، نسبت مولکولهای پرانرژی آب که قادر به تبخیر از سطح آب قند هستند، کمتر میباشد و در نتیجه فشار بخار محلول کمتر میشود.
▪ افزایش نقطه جوش
در اثر حل شدن مقداری حل شونده غیر فرار در یک حلال ، نقطه جوش آن افزایش مییابد. مقدار افزایش فقط به مقدار حل شونده بستگی دارد. برای مثال ، آب در شرایط متعارفی (دمای ۲۵درجه سانتیگراد و فشار بخار یک اتمسفر یا ۷۶۰میلی متر جیوه) در ۱۰۰درجه سانتیگراد می جوشد. اما اگر در آب، مقداری قند مثلا به غلظت یک مولال (یک مول در ۱۰۰۰گرم آب) بریزیم، فشار بخار محلول آب قند به اندازه ۱۴میلی متر جیوه کاهش مییابد و در نتیجه محلول در ۵۲/۱۰۰درجه سانتیگراد میجوشد.
▪ کاهش نقطه انجماد
وقتی یک حل شونده غیر فرار در یک حلال حل میشود، نقطه انجماد آن کاهش مییابد. بنابراین دمای انجماد محلولهای آبی همیشه کمتر از دمای انجماد آب خالص است. استفاده از این خاصیت در رادیاتور اتومبیل میباشد که برای جلوگیری از یخ زدن آب رادیاتور اتومبیل در زمستان ، به آن مقداری مایع به نام ضد یخ میافزایند. همچنین با اضافه کردن نمک (مانند کلرید سدیم) همراه با شن ریز روی آسفالت خیابانهای شهر ، هیدراته شدن یونهای نمکها مستلزم مصرف مقداری آب است که از ذوب شدن برف فراهم می گردد. بنابراین آب نمک غلیظی فراهم میشود که حتی در ۲۰درجه زیر صفر منجمد نمی شود.
▪ فشار اسمزی
اگر در ظرف U شکلی ، حلال A از مخلوط حلال و حل شونده (B + A) به وسیله یک غشای نیمه تراوا ، جدا شود، چون فقط حلال از غشا عبور میکند، بعد از رسیدن به حالت تعادل ، ارتفاع مایع در قسمت که حل شونده وجود دارد بالا می رود.
اگر به این ستون فشار وارد شود تا سطح مایع در دو طرف یکسان شود، این فشاراسمزی است که به علت حل شدن حل شونده غیر فرار در حلال ایجاد شده است.
به عکس فرآیند اسمز ، اسمز معکوس گویند که برای شیرین کردن آب استفاده می شود. همچنین برای تعیین جرم مولکولی پلیمرها ، پروتئینها و بطور کلی مولکولهای سنگین از فشار اسمزی استفاده میشود.
به نام یگانه خالق هستی
موضوع:اسیدها
گردآورنده:محمّدیوسفی
معلم مربوطه:آقای سلامی
کلاس دوم تجربی
دبیرستان شهید رجایی1
اسیدها
اسیدها موادی ترش مزه اند خاصیت خورندگی دارند شناساگرها را تغییر رنگ می دهند و بازها را خنثی می کنند.
● تعریف قدیمی
اسیدها موادی ترش مزه اند خاصیت خورندگی دارند شناساگرها را تغییر رنگ می دهند و بازها را خنثی می کنند.
بازها موادی با مزهٔ گس-تلخ اند حالتی لزج دارند شناساگرها را تغییر رنگ می دهند و اسیدها را خنثی می کنند.
▪ لی بیگ: اسیدها موادی اند که در ساختار خود هیدروژن یا هیدروژن هایی دارند که در واکنش با فلزها توسط یون های فلز جایگزین می شوند.
▪ آرنیوس: اسیدها موادی هستند که ضمن حل شدن در آب یون +H آزاد می کنند. بازها موادی هستند که ضمن حل شدن در آب یون -OH آزاد می کنند.این تعریف فقط به موادی محدود میشود که در آب قابل حل باشند. حدود سال ۱۸۰۰، شیمی دانان فرانسوی از جمله آنتوان لاووازیه، تصور می کرد که تمام اسیدها دارای اکسیژن هستند. شیمی دانان انگلیسی از جمله سر همفری دیوی، معتقد بود که تمام اسیدها دارای هیدروژن هستند. شیمی دان سوئدی، سوانت آرنیوس، از این عقیده برای گسترش تعریف اسید استفاده نمود.
▪ لوییس: اسیدها موادی هستند که در واکنش های شیمیایی پیوند داتیو می پذیرند. بازها موادی هستند که در واکنش های شیمیایی پیوند داتیو می دهند.تعریف لوییس را با نظریه اوربیتال مولکولی هم میتوان بیان کرد. به طور کلی، اسید میتواند یک جفت الکترون از بالاترین اوربیتال خالی در پایین اوربیتال خالی خود دریافت کند. این نظر را گیلبرت ن. لوییس مطرح کرد. با وجود این که این تعریف گسترده ترین تعریف است، تعریف لوری-برونستد کاربرد بیشتری دارد. با استفاده از این تعریف میتوان میزان قدرت یک اسید را هم مشخص نمود. از این مفهوم در شیمی آلی هم استفاده میشود (مثلاً در کربوکسیلیک اسید)
● نگاه اجمالی
بشر از دیر باز با مفهوم ساده اسید آشنایی داشته است. در حقیقت این مواد، حتی قبل از آنکه شیمی به صورت یک علم در آید، شناخته شده بودند. اسیدهای آلی همچون سرکه و آبلیمو و آب غوره از قدیم معروف بودند. اسیدهای معمولی مانند اسید سولفوریک ، اسید کلریدریک و اسید نیتریک بوسیله کیمیاگران قدیم ساخته شدند و بصورت محلول در آب بکار رفتند. برای مثال اسید سولفوریک را جابربن حیان برای نخستین بار از تقطیر بلورهای زاج سبز (FeSO۴.۷H۲O) و حل کردن بخارات حاصل در آب ، بدست آورد.
در طی سالیان متمادی بر اساس تجربیات عملی لاووازیه (A.L.Lavoisier) چنین تلقی میگردید که اجزاء ساختمان عمومی کلیه اسیدها از عنصر اکسیژن تشکیل گردیده است. اما بتدریج این موضوع از نظر علمی روشن و اعلام گردید که چنانچه این موضوع صحت داشته باشد، بر خلاف عقیده اعلام شده در مورد اکسیژن ، این عنصر هیدروژن است. در حقیقت ، تعریف یک اسید بنا به فرمول اعلام شده از سوی لیبیگ: (J. Von Liebig) در سال ۱۸۴۰عبارت است از
ـ موادی حاوی هیدروژن که میتوانند با فلزات واکنش نموده و گاز هیدروژن تولید نمایند.
ـ نظریه فوق مدت پنجاه سال مورد استناد بوده است. بعدها با پیشرفت علم شیمی ، مفاهیم جدیدی درباره اسیدها اعلام شده که در زیر به بررسی آنها خواهیم پرداخت.
● خواص عمومی اسیدها
▪ محلول آبی آنها یونهای پروتون آزاد میکند
▪ موادی هستند که از نظر مزه ترشند
▪ کاغذ تورنسل را سرخ رنگ میکنند
▪ با برخی فلزات مانند آهن و روی ترکیب شده گاز هیدروژن میدهند
▪ با قلیاها (بازها) واکنش نموده و املاح را تشکیل میدهند
با کربنات کلسیم (مثلا به صورت سنگ مرمر) بشدت واکنش دارند، بطوریکه کف میکنند و گاز کربنیک آزاد مینمایند.
● اکسیدهای اسیدی
اکسیدهای بسیاری از غیرفلزات با آب واکنش داده و اسید تولید میکنند، در نتیجه این مواد را اکسیدهای اسیدی یا ایندرید اسید مینامند.
N۲O۵(s) + H۲O → H+ + NO۳-aq
مفهوم آرنیوس ، به علت تاکید آن بر آب و واکنشهای محلولهای آبی ، با محدودیت روبهروست.
اسید ۲ + باز ۱ <----- اسید ۱ + باز ۲
قدرت اسیدها ، بر میل آنها برای از دست دادن یا گرفتن پروتون استوار است. هر چه اسید قویتر باشد، باز مزدوج آن ضعیفتر است. در یک واکنش ، تعادل در جهت تشکیل اسید ضعیفتر است. اسید پرکلریک ، HClO۴، قویترین اسید است، و باز مزدوج آن ، یعنی یون پرکلرات ، -ClO۴، ضعیفترین باز میباشد. H۲، ضعیفترین اسید و باز مزدوج آن یعنی یون هیدرید ، +H قویترین باز میباشد
● نظریه لوییس درباره اسیدها
گیلبرت لوییس مفهوم گستردهتری برای اسیدها در سال ۱۹۳۸پیشنهاد داد که پدیده اسید - باز را از پروتون رها ساخت. طبق تعریف لوییس ، اسید مادهای است که بتواند با پذیرش یک زوج الکترون از باز ، یک پیوند کوولانسی تشکیل دهد. در نظریه لوییس به مفهوم زوج الکترون و تشکیل پیوند کووالانسی تاکید میشود. تعریف لوییس در مورد اسیدها بسیار گستردهتر از آن است که برونشتد عنوان نموده است. ترکیبات شیمیایی که میتوانند نقش اسید لوییس داشته باشند، عبارتند از:
مولکولها یا اتمهایی که هشتتایی ناقص داشته باشند
(BH۳ + F- → BH۴-(aq
بسیاری از کاتیونهای ساده میتوانند نقش اسید لوییس داشته باشند.
Cu+۲ + ۴NH۳ → Cu(NH۳)۴+۲
برخی از اتمهای فلزی در تشکیل ترکیباتی مانند کربونیلها که از واکنش فلز با مونوکسید کربن تولید میشود، نقش اسید دارند.
Ni + ۴CO → Ni(CO)۴
ترکیباتی که اتم مرکزی آنها تونایی گسترش لایه ظرفیتی خود را داشته باشند ، در واکنشهایی که این گسترش عملی شود، نقش اسید دارند، مثلا در واکنش مقابل ، لایه ظرفیتی اتم مرکزی (Sn) از ۸به ۲الکترون گسترش یافتهاست.
SnCl۴ + ۲Cl- → SnCl۶-۲aq
برخی ترکیبات به علت داشتن یک یا چند پیوند دو گانه در مولکول ، خاصیت اسیدی دارند. مثلا CO۲
قدرت اسیدی و ساختار مولکولی.
به منظور بررسی رابطه بین ساختار مولکولی و قدرت اسیدی ، اسیدها را به دو نوع تقسیم میکنیم: هیدریدهای کووالانسی و اکسی اسیدها
● هیدریدها
برخی از ترکیبات کووالانسی دوتایی هیدروژن دار اسیدی هستند.دو عامل بر قدرت اسیدی هیدریدیک
عنصرموثر است:الکترونگاتیوی عنصرو اندازه اتمی عنصر.
قدرت اسیدی هیدریدهای عناصر یک گروه، با افزایش اندازه اتم مرکزی افزایش مییابد. در تناوب دومNH۳>H۲O>HF در گروه VIبه اینصورت است:
H۲Te > H۲Se > H۲S > H۲O
● اکسی اسیدها
در این ترکیبات ، هیدروژن اسیدی به یک اتم O متصل است و تغییر در اندازه این اتم بسیار ناچیز است. بنابراین عامل کلیدی در قدرت اسیدی این اکسیاسیدها، به الکترونگاتیوی اتم Z مربوط میشود
.H-O-Z
اگر Z یک اتم غیرفلز با الکترونگاتیوی بالا باشد، سهمی در کاهش چگالی الکترونی پیرامون اتم O (علی رغم الکترونگاتیوی شدید اکسیژن) را دارد. این پدیده باعث میشود که اتم اکسیژن، با کشیدن چگالی الکترونی پیوند H-O از اتم H ، تفکیک آن را سرعت ببخشد و ترکیب را اسیدی بکند. هیپوکلرواسید ، .HOCl اسیدی از این نوع است
● مهمترین اسیدهای قوی
مولکولهای این اسیدها و در محلولهای آبی رقیق کاملا یونیزه است. اسیدهای قوی متعارف عبارتند از: اسید کلریدریک ، یدیدریک ، نیتریک ، سولفوریک ، پرکلریک است.
● مهمترین اسیدهای ضعیف
یونیزاسیون این اسیدها در آب کامل نمیباشد و هرگز به ۱۰۰%نمیرسد. مثال متعارف آنها ، اسید استیک ، اسید کربنیک ، اسیدفلوریدریک ، اسید نیترو و تا حدودی اسید فسفریک است.
اسیدها مزه ترشی دارند بعضی اسیدها سمی هستند بعضی باعث سوختگی های شدید می شوند و تعدادی نیز کاملاً بی ضرر به شمار می آیند بعضی اسیدها نیز خوراکی و بسیار مفید هستند ما اسید سیتریک را از پرتقال و لیموترش به دست می آوریم بدنمان هم اسیدهایی را می سازند که به گوارش غذا کمک می کنند.
اسید سولفوریک یکی از قوی ترین و مهم ترین اسیدها است که به مقدار فراوان در تولید انواع کود ، فرآورده های نفتی و آهن و فولاد بکار گرفته می شوند آب باتری اتومبیل ها اسید سولفوریک رقیق شده با آب خالص است سایر اسیدهای قوی عبارتند از: اسید نیتریک و اسید کلرید ریک.
بازها یا قلیاها موادی هستند که مخالف و ضد اسیدها به شمار می آیند گرچه بعضی بازها از قبیل آهک (هیدروکسید کلسیم) و سود سوز آور همانند اسیدها خیلی فعال و خورنده هستند از بازها در فرآیند های صنعتی استفاده می شوند هیدروکسید منیزیم (مایع یا پودر سفیدی که برای برطرف کردن درد ناشی از حالت اسیدی معده مصرف می کنیم) نمونه ای از یک باز ملایم است بازی که در آن قابل حل می باشد ، قلیا نامیده می شود وقتی یک اسید و یک باز به نسبت مناسب با هم مخلوط می شوند یکدیکر را خنثی می کنند برای مثال اگر اسید کلرید ریک با سود سوز آور مخلوط شود حاصل واکنش آنها نمک معمولی و آب خواهد بود بعضی مواد وقتی با اسید و بازها تماس پی�
نام و نام خانوادگی:محمد تقی زاده
موضوع:نفت طلای سیاه
نام مدرسه:ملا صدرا 1
شعبه کلاس:06
نفت یا طلای سیاه چیست؟
نفت چیست؟
نفت مخلوطی است از هیدروکربن های جامد . مایع و گاز که از تجزیه شدن پیکر مرده ی جانداران تک سلولی . که میلیونها سال پیش می زیسته اند ، بوجود آمده است . در جستجوی نفت نفت ، آمیخته ای است از مواد شیمیایی آلی ، عمدتا از بقایای گیاهان و جانوران خرد و ریزی که میلیونها سال پیش در دریا می زیسته اند . شرایط و حالات ویژه و زمانهای بسیار دراز لازم بوده است تا این بقایا در معرض تغییر و تبدیل های پیچیده شیمیایی قرار گیرند و نتیجتا نفت و گاز ایجاد شود . گاه این توده مواد به نحوی در یک نقطه متمرکز می شود که انسان بتواند جای آن را کشف و از آن بهره برداری کند.
پلاتین (Pt)/مهران روشن/کلاس06/دبیرستان ملاصدرا یکاز عنصرها عدد اتمی این عنصر ۷۸ و نشانه اختصاری آن Pt است. پلاتین از گروه فلزات واسطه به رنگ سفید-خاکستری، متراکم، رسانا و شکلپذیر است و از باارزشترین فلزات گرانبها محسوب میشود. نام این فلز برگرفته از واژه اسپانیایی پلاتینا به معنی «نقره کوچک» است.
پلاتین کمترین واکنشپذیری در بین تمامی فلزات را دارد و همچنین مقاومت بسیار بالایی نسبت به خوردگی دارد و حتی در محیطهای بسیار داغ نیز این ویژگی را حفظ میکند. بیشتر کاربردهای پلاتین به دلیل این ویژگیها و خاصیت کاتالیزوری بالای آن است. بیشترین استفاده پلاتین در ساخت مبدلهای کاتالیست و جواهرات است. ابزارهای مخصوص آزمایشگاهی، اتصالهای الکتریکی و الکترودها، تجهیزات پزشکی و دندانپزشکی، دستگاههای مقاوم در برابر خوردگی و زنگزدگی، تجهیزات حرارتسنج برای کورههای الکتریکی، پوشش موشکها، و سوخت موتور جت از دیگر موارد استفاده این فلز است.
پلاتین از نادرترین عناصر در پوسته زمین است و غلظت آن فقط ۵ در میلیارد است. پلاتین به صورت آزاد در طبیعت وجود دارد و معمولاً همراه دیگر فلزهای خانواده پلاتین یعنی پالادیم، روتنیم، رودیم، ایریدیم و اسمیم دیده میشود. همگی این ۶ عنصر ویژگیهایی شبیه به هم دارند و عناصری بسیار نادر هستند.
تاریخچه
نخستین مورد شناختهشده از کاربرد پلاتین در تاریخ بشر به بومیان قاره آمریکا در کشور اکوادور کنونی برمیگردد که این فلز را از شنهای رودخانه به دست آورده و از آلیاژ پلاتین و طلا برای ساخت زینتآلات استفاده میکردند. ژولیوس سزار اسکالیگر مردمشناس ایتالیایی در سال ۱۵۵۷ نخستین اروپایی بود که وجود این فلز را گزارش کرد. وی آن را فلزی توصیف کرده بود؛ «که نه آتش و نه هیچ ابزار اسپانیایی قادر به ذوب کردن آن نیست». این توصیف اشاره به دمای بالای ذوب این فلز دارد. نقطه ذوب پلاتین ۱۷۶۸ درجه سانتیگراد و نقطه جوش آن در ۳۸۲۵ درجه است.
تولید
پلاتین در نهشتههای آبرفتی و به ویژه نهشتههای نیکلی دیده میشود و به عنوان فرآورده ثانویه معادن نیکل و مس به دست میآید. تولید جهانی پلاتین در سال ۲۰۱۰ حدود ۱۹۲ تن بودهاست که که معادل کمتر از یکسیزدهم تولید طلا در همان سال است. حدود ۷۷٪ از این میزان در آفریقای جنوبی تولید شده است. روسیه ۱۳ درصد تولید پلاتین دنیا را به خود اختصاص داده و کانادا، زیمباوه و آمریکا هم در رتبههای بعدی قرار گرفتهاند.
مجموعه معادن سنگهای آذرین بوچولد در آفریقای جنوبی بیشترین تولید پلاتین و بیشترین ذخیره پلاتین و دیگر سنگهای گروه پلاتین دنیا را به خود اختصاص دادهاند. معدن سنگهای آذرین نیکل و مس در نزدیکی شهر نوریلسک در روسیه و معدن نیکل حوضه سادبری در کانادا که بر اثر برخورد شهابسنگ ایجاد شده، دو ذخیرهگاه عمده دیگر پلاتین هستند. سنگهای معدن سادبری فقط نیم گرم در هر تن پلاتین دارند و حجم عظیم استخراج نیکل این معادن است که تولید پلاتین را اقتصادی میکند. معادن کوچکتری هم در ایالتهای غربی آمریکا قرار دارند. معدنی در کلمبیا که از زمان پیش از ورود اروپاییان از آن برداشت میشده هم هنوز به تولید خود ادامه میدهد.
قیمت
قیمت پلاتین از طلا نوسان بیشتری دارد. این فلز معمولا در وضعیت ثبات و رشد اقتصادی گرانتر از طلاست و قیمت آن تا دو برابر طلا میرسد اما در دورههای بیثباتی اقتصادی گاهی از طلا ارزانتر میشود. چراکه پلاتین در درجه اول کاربرد صنعتی دارد و در زمان رشد اقتصادی تقاضای آن افزایش پیدا میکند در حالی که طلا بیشتر کاربرد سرمایهگذاری دارد و در زمان ناآرامی اقتصادی تقاضای آن بیشتر میشود. مثلا در جریان رکود اقتصادی سال ۲۰۰۸ قیمت پلاتین از ۲۲۵۲ دلار برای هر اونس تروا (۳۱.۱ گرم) به ۷۷۴
به نام خدا
نام و نام خانوادگی:ماهان رهنما.
نام دبیر:آقای سلامی.
موضوع:لایه اوزون.
کلاس:06(سال اول).
دبیرستان:ملاصدرا(1).
تعریف کلی
اتم اکسیژن و مولکول اکسیژن (O2) دارای دو اتم اکسیژن است اما اختلاف یک اتم اکسیژن در این دو مولکول تفاوتهای اساسی را بین آنها بوجود آورده است.
بسم الله الرحمن الرحیم
فیبرنوری(optical fiber)
نیما حاجیان/کلاس06/دبیرستان ملاصدرا یک/دبیرآقای سلامی فیبر نوری یا تار نوری رشتهٔ باریک و بلندی از یک مادّهٔ شفاف مثل شیشه یا پلاستیک است که میتواند نوری را که از یک سرش به آن وارد شده، از سر دیگر خارج کند. فیبر نوری داری پهنای باند بسیار بالاتر از کابلهای معمولی میباشد، با فیبر نوری میتوان دادههای تصویر، صوت و دادههای دیگر را به راحتی با پهنای باند بالا تا ۱۰ گیگابیت بر ثانیه و بالاتر انتقال داد. امروزه مخابرات فیبر نوری، به دلیل پهنای باند وسیعتر در مقایسه با کابلهای مسی، و تاخیر کمتر در مقایسه با مخابرات ماهواره ای از مهمترین ابزار انتقال اطلاعات محسوب میشود.
تاریخچهٔ ساخت فیبر نوری
اولین کسانی که در قرون اخیر به فکر استفاده از نور برای انتقال اطلاعات افتادند، انتشار نور را در جو زمین تجربه کردند. اما وجود موانع مختلف نظیر گرد و خاک، دود، برف، باران، مه و... انتشار اطلاعات نوری در جو را با مشکل مواجه ساخت. بعدها استفاده از لوله و کانال برای هدایت نور مطرح گردید. نور در داخل این کانالها بوسیله آینهها و عدسیها هدایت میشد، اما از آنجا که تنظیم این آینهها و عدسیها کار بسیار مشکلی بود این کار نیز غیر عملی تشخیص داده شد و مردود ماند.
شاید اولین تلاش در سیر تکاملی سیستم ارتباط نوری به وسیله الکساندر گراهام بل صورت گرفت که در سال ۱۸۸۰، درست ۴ سال پس از اختراع تلفن، اختراع تلفن نوری (فوتوفون) یا سیستمی که صدا را تا فواصل چندین صد متر منتقل می کرد، به ثبت رساند. تلفن نوری بر مبنای مدوله کردن نور خورشید بازتابیده با به ارتعاش در آوردن آینه ای کار می کرد. گیرنده یک فتوسل بود. در این روش نور در هوا منتشر می شد و بنابراین امکان انتقال اطلاعات تا بیش از ۲۰۰ متر میسر نبود. به همین دلیل، اگرچه دستگاه بل ظاهراً کار می کرد اما از موفقیت تجاری برخوردار نبود.
ایده استفاده از انکسار (شکست) برای هدایت نور (که اساس فیبرهای نوری امروزی است) برای اولین بار در سال ۱۸۴۰ توسط Daniel Colladon و Jacques Babinet در پاریس پیشنهاد شد. همچنین John Tyndall در سال ۱۸۷۰ در کتاب خود ویژگی بازتاب کلی را شرح داد: «وقتی نور از هوا وارد آب می شود به سمت خط عمود بر سطح خم میشود و وقتی از آب وارد هوا می شود از خط عمود دور می شود. اگر زاویه ی پرتو نور با خط عمود در تابش از داخل آب بزرگتر از ۴۸ درجه شود هیچ نوری از آب خارج نمیشود در واقع نور به طور کامل از سطح آب منعکس می شود. زاویه ای که انعکاس کلی آغاز می شود را زاویه بحرانی می نامیم».
کاکو و کوکهام انگلیسی برای اولین بار استفاده از شیشه را بعنوان محیط انتشار مطرح ساختند. آنان مبنای کار خود را بر آن گذاشتند که به سرعتی حدود ۱۰۰ مگابیت بر ثانیه و بیشتر بر روی محیطهای انتشار شیشه دست یابند. این سرعت انتقال با تضعیف زیاد انرژی همراه بود. این دو محقق انگلیسی، کاهش انرژی را تا آنجا میپذیرفتند که کمتر از ۲۰ دسی بل نباشد. اگر چه آنان در رسیدن به هدف خود ناکام ماندند، اما شرکت آمریکائی (کورنینگ گلس) به این هدف دست یافت. در اوایل سال ۱۹۶۰ میلادی با اختراع اشعه لیزر ارتباطات فیبرنوری ممکن گردید. در سال ۱۹۶۶ میلادی، دانشمندان در این نظریه که نور در الیاف شیشهای هدایت میشود پیشرفت کردند که حاصل آن از کابلهای معمولی بسیار سودمندتر بود. چرا که فیبرنوری بسیار سبکتر و ارزانتر از کابل مسی است و در عین حال ظرفیت انتقالی تا چندین هزار برابر کابل مسی دارد.
توسعه فناوری فیبرنوری از سال ۱۹۸۰ میلادی به بعد باعث شد که همواره مخابرات نوری بعنوان یک انتخاب مناسب مطرح باشد. تا سال ۱۹۸۵ میلادی در دنیا نزدیک به ۲ میلیون کیلومتر کابل نوری نصب شده و مورد بهره برداری قرار گرفتهاست.
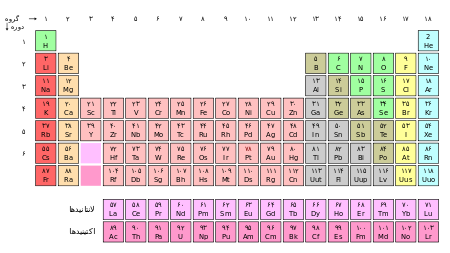
خواص تناوبی عنصرها
مندلیف پس از سالها مطالعه متوجه شده که اگر عنصرها را بر حسب افزایش تدریجی جرم آنها در ردیفهای کنار یکدیگر بگذارد و آنهایی را که خواص فیزیکی و شیمیایی نسبتاً مشابه دارند در یک گروه زیر یکدیگر قرار دهد، عنصرها به ترتیبی سازماندهی می شوند که خواص آنها با نظم و ترتیب خاص تغییر می کند. اما در جدول مندلیف در چند مورد نیز بی نظمی هایی مشاهده می شد، زیرا او مجبور بود در مواردی در یک ستون قرار دادن عنصرهایی با خواص مشابه . ترتیب قرار گرفتن عنصرها بر اساس افزایش جرم نادیده بگیرد.
جواد ستایش مدرسه شهید نصیری کلاس 05
الوتروپی یا چند شکلی خاصیتی از عناصر شیمیایی مشخصی است که درحالت های فیزیکی یکسان (گاز ‚ مایع
‚ جامد) دارای دو یاچند شکل مختلف هستند. برخی از شکل های الوتروپی یا الوتروپ ها بر اثر تفاوت های تعداد اتم های
موجود در یک مولکول یک عنصر میباشد. همانند اکسیژن معمولی با فرمول O2و اکسیژن سه اتمی یا اوزون با فرمول O3
همچنین الوتروپی میتواند به علت چیدمان متفاوت اتم ها در ساختار بلورین یا غیر بلورین (بی نظم) یک عنصر باشد.
به طور مثال کربن در شکل های الوتروپی بلورین متفاوت به صورت الماس و گرافیت وجود دارد. خاصیت بلوری در دو یا
چند شکل با اصطلاح چند ریختی (Polymorphism) شناخت میشوند.
تعداد دیگری از عناصر از جمله قلع ‚ اهن ‚ سلنیوم ‚ فسفر و گوگرد دارای الوتروپ هایی هستند که به علت چیدمان
متفاوت اتم های ان ها حاصل میشود.
به نام خدا
تحقیقی از : جواد میرزاخواه
موضوع : اکسایش
اُکسایــِش و کاهش (به انگلیسی: Redox) نام کلی واکنشهای شیمیایی است که مایه تغییر عدد اکسایش اتمها میشوند. این فرایند میتواند دربرگیرنده واکنشهای سادهای همچون اکسایش کربن و تبدیل آن به کربن دیاکسید و کاهش کربن و تبدیل آن به متان و یا واکنشهای پیچیدهای چون اکسایش قند در بدن انسان طی واکنشهای چند مرحلهای باشد
به نام خدا
تحقیقی از : جواد میرزاخواه
موضوع : پیوند داتیو
پیوند داتیو نوعی پیوند کووالانسی بین دو اتم است که دو الکترون از یک اتم وارد اربیتال خالی اتم دیگر میشوند
به نام خدا
تحقیقی از : جواد میرزاخواه
موضوع : اتم اسکاندیم
اسکاندیم(Scandium) از عنصرهای شیمیاییجدول تناوبی است. نشانه کوتاه آن Sc و عدد اتمی آن ۲۱ است.
کسری نادم مدرسه ملاصدرا کلاس 05
آلودگى هوا به معناى مخلوط شدن هوا با گازها،قطرات و ذراتى است كه كيفيت هوا را كاهش مىدهند
در شهرها، ماشينها و اتوبوسها، هواپيماها و نيز صنايع و ساختمانسازى ممكن است باعث آلودگى هوا شوند.
به نام خدا
نویسندگان : رضا آقایی و محمد جهانی
سرب استفنات (lead styphnate) از مواد بسیار مفیدی در امر تخریب است که امروزه از آن در چاشنی ها استفاده می گردد حساسیت این ماده همانند استیلید نقره است و دارای سرعت انفجاری برابر با ۴۹۰۰ متر بر ثانیه است این ماده هم خانواده سرب پیکرات است ولی به مراتب ایمن تر و قوی تر از آن است ساخت این ماده پر خرج بوده و دارای مراحل زیادی است و می بایستی از مواد شیمیایی با درجه خلوص بسیار بالا استفاده کرد
این ماده برخلاف اسید پیکریک با فلزات واکنش نداده و کاملا در آب و متیل الکل(متانول) محلول است حساسیت آن نسبت به فولمینات جیوه و نیترید سرب کمتر است و جزو مواد انفجاری با حساسیت زیاد طبقه بندی می شود
این ماده یکی از گزینه های عالی برای چاشنی ها و دیگران تجهیزات انفجاری است.
ساخت این ماده به دو روش میسر است
۱- استفاده از استفنات اسید
۲- استفاده از استفنات منیزیم
من شخصا روش اول را پیشنهاد می کنم چون به نظر من مواد تشکیلی دارای درجه خلوص بالایی است ولی بهر حال در صورت نیاز می توانم روش دوم را نیز توضیح دهم.(روش دوم ساده تر است در صورتی که استفنات منیزیم پیدا شود)
علت اصلی که تولید این ماده را از روش اول توضیح می دهم آن است که در روش اول می بایستی استفنات اسید تولید شود که خود این ماده را نیز می توان در ترکیبات مفید دیگری نیز وارد کرد و ترکیبات سودمندی را بدست آورد.(پتاسیم استفنات-نقره استفنات و...)
مواد و تجهیزات مورد نیاز:
۱- رزورسینول (resorcinol) ۱۰۰ گرم
(این ماده از لحاظ ساختاری شبیه به فنول است با این تفاوت که یک گروه OH اضافه تر دارد)
۲- اسید نیتریک ۶۵% ۳۰۰ سی سی
۳- اسید سولفوریک ۹۸% ۳۰۰ سی سی
۴- اکسید سرب (II) ۴۰ گرم
۵- دماسنج ۱ عدد
۶- دستکش
۷- کاغذ یا پارچه صافی
۸- بشر ۱۰۰۰ سی سی ۲ عدد
۹- همزن شیشه ای
۱۰- متانول ۴۰۰ سی سی
در مرحله اول شما می بایستی استفنات اسید را تهیه کنید که طرز تهیه آن همانند طریقه ساخت اسید پیکریک است با این تفاوت که شما می بایستی بجای استفاده از آسپیرین و حل کردن آن در محلول اسید مستقیما رزورسینول را به اسید سولفوریک گرم اضافه کنید و سپس عینا تکرار مراحل تولید اسید پیکریک را تکرار کنید
در صورت نیاز به تولید این ماده نیز می پردازم
مراحل زیر را از تولید و خشک کردن استفنات اسید به بعد توضیح می دهم
۱- ۵۰ گرم استفنات اسید را در ۴۰۰ میلی لیتر متانول گرم حل می کنیم و با استفاده از هم زن شیشه ای محلول را هم می زنیم تا استفنات کاملا در اتانول حل شود(در صورتی که هنوز مقداری استفنات اسید در ته ظرف باقی ماند به مقدار متانول اضافه می کنیم)
۲- به آرامی ۴۰ گرم اکسید سرب را به محلول اضافه کرده و به مدت ۳۰ دقیق محلول را هم می زنیم.
۳-اجازه می دهیم تا محلول به مدت ۱ ساعت در جایی مطمین باقی بماند تا کریستال های سرب استفنات بطور کامل رسوب شود.
۴-با استفاده از کاغذ صافی یا پارچه محلول را فیلتر کرده و سرب استفنات را جدا می کنیم
۵- اجازه می دهیم تا رسوب به مدت ۴۸ ساعت در دمای اتاق در مکانی امن قرار گیرد تا خشک شود.
پس از گذشت این زمان ماده ما آماده است و می توان آن را در چاشنی و دیگر لوازم انفجار دیگر پر کرد.
این ماده را جهت نگهداری می بایستی همانند فولمینات جیوه و دیگر ترکیبات در آب نگهداری کرد
تعداد صفحات : 26