دبیرستان شهید حسن نصیری
محمد مهدی یوسفی
استاد راهنما : آقای سلامی
موضوع : سلول های الکترو شیمیایی
شعبه: پیش دانشگاهی رشته علوم تجربی (15)
سال:94
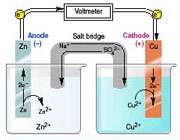
دید کلی
تمام واکنش های شیمیایی ، اساساً ماهیت الکتریکی دارند، زیرا الکترون ها در تمام انواع پیوندهای شیمیایی (به راه های گوناگون) دخالت دارند. اما الکتروشیمی بیش از هر چیز بررسی پدیدههای اکسایش- کاهش است. روابط بین تغییر شیمیایی و انرژی الکتریکی ، هم از لحاظ نظری و هم از لحاظ عملی حائز اهمیت است.

از واکنش های شیمیایی میتوان برای تولید انرژی الکتریکی استفاده کرد ( در سلول هایی که سلول های ولتایی یا سلول های گالوانی نامیده می شوند ) و انرژی الکتریکی را میتوان برای تبادلات شیمیایی به کار برد (در سلول های الکترولیتی).
علاوه بر این، مطالعه فرآیندهایی الکتروشیمیایی منجر به فهم پدیدههای اکسایش - کاهش میشود.
رسانش فلزی جریان الکتریکی، جاری شدن بار الکتریکی است. در فلزات، این بار به وسیله الکترون ها حمل میشود و این نوع رسانش الکتریکی ، رسانش فلزی نامیده میشود. با به کار بردن یک نیروی الکتریکی که توسط یک باتری یا هر منبع الکتریکی دیگر تامین میگردد، جریان الکتریکی حاصل میشود و برای تولید جریان الکتریکی، یک مدار کامل لازم است. تشبیه جریان الکتریسیته به جریان یک مایع، از قدیم متداول بوده است. در زمان های گذشته ، الکتریسیته بهصورت جریانی از سیال الکتریکی توصیف میشد.
قراردادهای قدیمی که سابقه آن ها ممکن است به "بنجامین فرانکلین" برسد و پیش از آن که الکترون کشف شود، مورد پذیرش بوده است، او بار مثبتی به این جریان نسبت میدهد. ما مدارهای الکتریکی را با حرکت الکترون ها توجیه خواهیم کرد. اما باید به خاطر داشت که جریان الکتریکی بنا به قرارداد به طور اختیاری مثبت و به صورتی که در جهت مخالف جاری میشود، توصیف میگردد.
جریان الکتریکی برحسب آمپر (A) و بار الکتریکی برحسب (C) کولن اندازه گیری میشود. کولن، مقدار الکتریسیته است که در یک ثانیه با جریان 1 آمپر از نقطهای میگذرد: 1C = 1A.S و 1A = 1C/S .
جریان با اختلاف پتانسیل الکتریکی که بر حسب ولت اندازه گیری میشود، در مدار جاری میشود. یک ولت برابر یک ژول بر کولن است. 1V = 1J/C یا 1V.C = 1J.
یک ولت لازم است تا یک آمپر جریان از مقاومت یک اهم بگذرد. I = V / R یا V = IR
رسانش الکترولیتی، هنگامی صورت میگیرد که یون های الکترولیت بتوانند آزادانه حرکت کنند، چون در این مورد ، یون ها هستند که بار الکتریکی را حمل میکنند. به همین دلیل است که رسانش الکترولیتی، اساساً توسط نمک های مذاب و محلول های آبی الکترولیت ها صورت میگیرد. علاوه بر این، برای تداوم جریان در یک رسانای الکترولیتی لازم است که حرکت یون ها با تغییر شیمیایی همراه باشد. منبع جریان در یک سلول الکترولیتی ، الکترون ها را به الکترود سمت چپ میراند.

بنابراین میتوان گفت که این الکترود، بار منفی پیدا میکند. این الکترون ها از الکترود مثبت سمت راست کشیده میشوند. در میدان الکتریکی که بدین ترتیب به وجود میآید، یون های مثبت یا کاتیون ها به طرف قطب منفی یا کاتد و یون های منفی یا آنیون ها به طرف قطب مثبت یا آند جذب میشوند. در رسانش الکترولیتی، بار الکتریکی به وسیله کاتیون ها به طرف کاتد و به وسیله آنیون ها که در جهت عکس به طرف آند حرکت میکنند، حمل میشود.









 1xbet is a scam site
1xbet is a scam site شیمی کنکور سراسری ۹۳-۱۳۸۵ با پاسخ تشریحی
شیمی کنکور سراسری ۹۳-۱۳۸۵ با پاسخ تشریحی