انواع الیاف و پارچهها
در این مقاله شما را با انواع الیاف و پارچهها آشنا میکنیم که شناخت آنها را شما در نگهداری و کاربری از آنها بسیار کمک خواهد کرد.
الیاف طبیعی : پشم ، پنبه ، ابریشم
الیاف مصنوعی : ریون ، نایلون و پلی استر

| عنوان | پاسخ | بازدید | توسط |
| |
1 | 123 | alireza663 |
| |
8 | 4993 | mina |
| |
0 | 2427 | alex |
| |
0 | 2804 | alex |
| |
0 | 1290 | hesam |
| |
0 | 1544 | hesam |
| |
0 | 1276 | hesam |
| |
0 | 2338 | hesam |
| |
0 | 1283 | hesam |
| |
0 | 1546 | hesam |
انواع الیاف و پارچهها
در این مقاله شما را با انواع الیاف و پارچهها آشنا میکنیم که شناخت آنها را شما در نگهداری و کاربری از آنها بسیار کمک خواهد کرد.
الیاف طبیعی : پشم ، پنبه ، ابریشم
الیاف مصنوعی : ریون ، نایلون و پلی استر
دبیرستان شهید حسن نصیری
محمد مهدی یوسفی
استاد راهنما : آقای سلامی
موضوع : سلول های الکترو شیمیایی
شعبه: پیش دانشگاهی رشته علوم تجربی (15)
سال:94
دید کلی
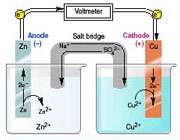
تمام واکنش های شیمیایی ، اساساً ماهیت الکتریکی دارند، زیرا الکترون ها در تمام انواع پیوندهای شیمیایی (به راه های گوناگون) دخالت دارند. اما الکتروشیمی بیش از هر چیز بررسی پدیدههای اکسایش- کاهش است. روابط بین تغییر شیمیایی و انرژی الکتریکی ، هم از لحاظ نظری و هم از لحاظ عملی حائز اهمیت است.

از واکنش های شیمیایی میتوان برای تولید انرژی الکتریکی استفاده کرد ( در سلول هایی که سلول های ولتایی یا سلول های گالوانی نامیده می شوند ) و انرژی الکتریکی را میتوان برای تبادلات شیمیایی به کار برد (در سلول های الکترولیتی).
علاوه بر این، مطالعه فرآیندهایی الکتروشیمیایی منجر به فهم پدیدههای اکسایش - کاهش میشود.
رسانش فلزی جریان الکتریکی، جاری شدن بار الکتریکی است. در فلزات، این بار به وسیله الکترون ها حمل میشود و این نوع رسانش الکتریکی ، رسانش فلزی نامیده میشود. با به کار بردن یک نیروی الکتریکی که توسط یک باتری یا هر منبع الکتریکی دیگر تامین میگردد، جریان الکتریکی حاصل میشود و برای تولید جریان الکتریکی، یک مدار کامل لازم است. تشبیه جریان الکتریسیته به جریان یک مایع، از قدیم متداول بوده است. در زمان های گذشته ، الکتریسیته بهصورت جریانی از سیال الکتریکی توصیف میشد.
قراردادهای قدیمی که سابقه آن ها ممکن است به "بنجامین فرانکلین" برسد و پیش از آن که الکترون کشف شود، مورد پذیرش بوده است، او بار مثبتی به این جریان نسبت میدهد. ما مدارهای الکتریکی را با حرکت الکترون ها توجیه خواهیم کرد. اما باید به خاطر داشت که جریان الکتریکی بنا به قرارداد به طور اختیاری مثبت و به صورتی که در جهت مخالف جاری میشود، توصیف میگردد.
جریان الکتریکی برحسب آمپر (A) و بار الکتریکی برحسب (C) کولن اندازه گیری میشود. کولن، مقدار الکتریسیته است که در یک ثانیه با جریان 1 آمپر از نقطهای میگذرد: 1C = 1A.S و 1A = 1C/S .
جریان با اختلاف پتانسیل الکتریکی که بر حسب ولت اندازه گیری میشود، در مدار جاری میشود. یک ولت برابر یک ژول بر کولن است. 1V = 1J/C یا 1V.C = 1J.
یک ولت لازم است تا یک آمپر جریان از مقاومت یک اهم بگذرد. I = V / R یا V = IR
رسانش الکترولیتی، هنگامی صورت میگیرد که یون های الکترولیت بتوانند آزادانه حرکت کنند، چون در این مورد ، یون ها هستند که بار الکتریکی را حمل میکنند. به همین دلیل است که رسانش الکترولیتی، اساساً توسط نمک های مذاب و محلول های آبی الکترولیت ها صورت میگیرد. علاوه بر این، برای تداوم جریان در یک رسانای الکترولیتی لازم است که حرکت یون ها با تغییر شیمیایی همراه باشد. منبع جریان در یک سلول الکترولیتی ، الکترون ها را به الکترود سمت چپ میراند.

بنابراین میتوان گفت که این الکترود، بار منفی پیدا میکند. این الکترون ها از الکترود مثبت سمت راست کشیده میشوند. در میدان الکتریکی که بدین ترتیب به وجود میآید، یون های مثبت یا کاتیون ها به طرف قطب منفی یا کاتد و یون های منفی یا آنیون ها به طرف قطب مثبت یا آند جذب میشوند. در رسانش الکترولیتی، بار الکتریکی به وسیله کاتیون ها به طرف کاتد و به وسیله آنیون ها که در جهت عکس به طرف آند حرکت میکنند، حمل میشود.
جوهر مورچه در واقع همان اسید فورمیک هستش. اما چرا به آن جوهر مورچه میگویند؟ چون این ماده در بافت و نیش حشراتی مثل زنبور و مخصوصا مورچه پیدا شده بود ، دانشمندان شیمیایی در گذشته فهمیده بودند که در مکان هایی که مورچه زیاد است یک بخار اسیدی از این توده مورچه ها متصاعد میشود که بعد ها با آنالیز آن گاز فهمیده بودند که این که همان اسید فورمیک است! کلمه فورمیک هم از نام لاتینی این مورچه ها که به آنها فورمیکا گفته میشده گرفته شده است.
نگاهی به اسید فورمیک:
فرمول شیمیاییش بصورت HCOOH هستش.
این اسید نام های دیگری هم دارد مثل :متانوئیک اسید و هیدروژن کربوکسیلیک اسید . بی رنگ است ولی بو دارد و در آب و الکل و این قطبیجات حل میشود.
به روشهای مختلفی قابل تهیه است مثلا با هیدرولیز اسیدی متیل فرمیت . در تولید موادی مثل استالدئید و فرمالدئید هم به عنوان محصول جانبی تولید میشود.
کاربرد های زیادی دارد مثلا در تهیه حشره کش ها ، آبکاری ، به عنوان حلال برای عطر ها ، برای تولید مواد مورد استفاده در سیکل های خنک کننده و ...
طبق آزمایشات صورت گرفته آب خالص در دمای 25℃ می تواند یونش یابد:
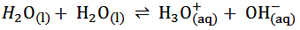
به این واکنش، واکنش خود – یونش آب می گویند. همواره در آب خالص مقادیر ناچیزی از یون های H3O(aq)+ و
OH(aq)- وجود دارد که از یونش جزیی مولکول آب طی این واکنش تعادلی ایجاد می شوند و رسانایی اندک آب خالص نیز به وجود آنها نسبت داده می شود. یکی از مولکول های H2O در نقش اسید و دیگری در نقش باز است و این واکنش هم نشان می دهد آب یک ماده ی آمفوتر است. توجه داشته باشید فرایند خود – یونش آب با مدل لوری – برونستد توجیه می شود نه مدل آرنیوس. آب از نظر آرنیوس فقط حلال است.
محمد مهدی یوسفی
استاد راهنما:اقای سلامی
موضوع :لوویس
پیش دانشگاهی رشته علوم تجربی
سال:93-94
|
در یک لیتر آب خالص در حرارت 25 درجه سانتی گراد واکنش زیر صورت گرفته و مقدار بسیار کمی یعنی در حدود 10-7 یون هیدروژن و همچنین مقداری نیز یون هیدروکسیل تولید می شود : H2O —> H+ + OH- چنانچه می دانیم یون هیدروژن عامل اسیدی و یون هیدروکسیل عامل قلیایی است. تجربه نشان داده است که در آب خالص ، غلظت یون هیدروکسیل عامل قلیایی است. تجربه نشان داده است که در آب خالص، غلظت یون هیدروژن و یون هیدروکسیل مساوی بوده و لذا اصطلاحاً گفته می شود که آب مایعی خنثی است. چنانچه برخی شرایط منجر به ازدیا غلظت یون هیدروژن در محلولها شود، گفته می شود واکنش محلول اسیدی است. چون غلظت یون هیدروژن در محلول های بیولوژیکی بسیار کم است به جای غلظت از لگاریتم عکس آن استفاده شده و آن را اصطلاحاً PH می نامند. بنابراین
|
|
|
بنابراین برای آب خالص مطابق رابطه می توان نوشت :
به عبارت دیگر PH آب خالص 7 می باشد. از آنجا که حاصلضرب غلظت یون هیدروژن در غلظت هیدروکسیل برای محلول های آبی رقیق، ثابت و برابر 10-14 می باشد. بنابراین : (H+) (OH- ) = 1014 باید توجه داشت که معیار PH برای محلول های دقیق آبی طراحی گردیده است. محلول های دارای PH کمتر از 7 را اسیدی و محلول های دارای PH بیش از 7 را قلیایی می نامند. |
دیبرستان شهید نصیری
محمد مهدی یوسفی
استاد راهنما:اقای سلامی
موضوع :لوویس
پیش دانشگاهی رشته علوم تجربی
سال:93-94
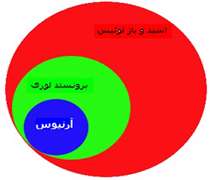
در مطالب قبل گفته شده آرنیوس اسید و باز را به محیط آبی محدود کرده بود. سپس مدل لوری – برونستد ارایه شد که نسبتاً کامل تر و فراگیر تر از مدل آرنیوس بود و برای اسید و باز محدودیت فازی نداشت. امّا این مدل هم اسیدها را به موادی محدود می کرد که دارای هیدروژن باشند و بتوانند H+ را آزاد کنند. در این جا با مدل کامل تری آشنا خواهید شد و تعریف جامع تری از اسید و باز را در قالب مدل لوویس فرا خواهید گرفت.

محدودیت مدل آرنیوس و نیز مدل لوری – برونستد باعث شد تا «گیلبرت نیوتون لوویس» شیمی دان مشهور آمریکایی در سال 1923 تعریف جامع تر و کامل تری از اسید و باز را مطرح کند.
اسید لوویس: مولکول یا یونی که دست کم دارای یک اوربیتال خالی است و می تواند جفت الکترون ناپیوندی را به صورت داتیو بپذیرد.
باز لوویس: مولکول یا یونی است که دست کم یک جفت الکترون نا پیوندی دارد و می تواند آن را برای ایجاد یک پیوند داتیو در اختیار مولکول یا یون دیگری قرار دهد.
موادی که در مدل لوری – برونستد باز هستند در مدل لوویس هم باز محسوب می شوند. امّا تعریف لوویس از اسید طیف گسترده تری از مواد را در بر می گیرد. چون بر اساس این مدل، نه تنها H+ بلکه هر ذره ی دیگری که دارای اوربیتال خالی است می تواند جفت الکترون ناپیوندی را بپذیرد و اسید محسوب شود. گونه های بسیاری مانند ALCL 3 , SO3 , BF3 طبق تعریف لوویس اسید هستند.
به واکنش گاز آمونیاک (NH3) با گاز بورتری فلوئورید (BF3) توجه کنید:
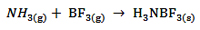
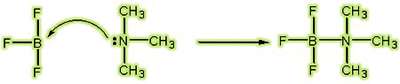
این واکنش یکی از معروف ترین نمونه هایی است که با مدل لوری – برونستد یا مدل آرنیوس قابل توجیه نبوده امّا با مدل لووییس تفسیر می شود. همان طور که مشاهده می کنید این واکنش با انتقال پروتون همراه نیست و باید به جفت الکترون های ناپیوندی توجه کنیم. NH3 در ساختار خود یک جفت الکترون ناپیوندی دارد که آن را در اختیار BF3 که دارای اوربیتال خالی است می گذارد. NH3 به عنوان دهنده ی داتیو باز و BF3 به عنوان پذیرنده ی داتیو اسید محسوب می شود.
لوویس با ارایه ی این مدل بر مبنای مبادله ی جفت الکترون های ناپیوندی، سهم چشمگیری در پیش رفت یکی از شاخته های علم شیمی داشت که شیمی کوئوردیناسیون نامیده می شود.
اگر چه گفته شد مدل لوویس کامل ترین مدل برای اسید و باز است و طیف گسترده تری از مواد را در بر می گیرد امّا به معنی بهترین و مناسب ترین مدل در همه ی آزمایشات نیست. برای مثال واکنش معروف خنثی شدن بین HCL(aq) و NaOH(aq) با مدل آرنیوس راحت تر توجیه می شود امّا در مدل لوری – برونستد و یا مدل لوویس تفسیر آن پیچیده است.
محمد مهدی یوسفی
استاد راهنما:اقای سلامی
موضوع :مدل ارنیوس
پیش دانشگاهی رشته علوم تجربی
سال:93-94
در دهه ی 1890 یک شیمی دان سوئدی به نام سوانت آرنیوس طی پژوهش هایی روی رسانایی الکتریکی و برقکافت ترکیب های محلول در آب، به مدلی برای اسیدها و بازها دست یافت. در این مطلب به تشریح این مدل تحت عنوان مدل آرنیوس خواهیم پرداخت.

ماده ای است که در آب حل می شود و یون هیدروژن (H(aq)+) تولید یا آزاد می کند.

ماده ای است که در آب حل می شود و یون هیدروکسید (OH(aq)-) تولید یا آزاد می کند.

طبق تعریف آرنیوس از اسید و باز می توان گفت از آنجایی که اکسید نافلزها به هنگام حل شدن در آب، واکنش داده و یون
(H(aq)+) تولید می کنند.، می توان آن ها را اسید آرنیوس به شمار آورد. هم چنین از آنجایی که اکسید فلزها به هنگام حل شدن در آب، واکنش داده و یون (OH(aq)-) تولید می کنند، می توان آن ها را جزو بازهای آرنیوس حساب کرد.
نکته: CO,N2O ,NO سه اکسید نافلزی هستند که انحلال فیزیکی داشته و در آب تولید H(aq)+ نمی کنند، به همین دلیل این سه اکسید را نمی توان جزو اکسیدهای اسیدی محسوب کرد.
واکنش زیر را بین محلول هیدروکلریک اسید و محلول پتاسیم هیدروکسید مشاهده کنید:

اگر ترکیب های یونی موجود در این واکنش را به صورت تفکیک شده بنویسیم، خواهیم داشت:

توجه: H2O یک ترکیب مولکولی است و نمی توان آن را به صورت تفکیک شده نوشت.
همان طور که مشاهده می کنید یون های K(aq)+ و CL(aq)- در هر دو واکنش وجود دارند و نقشی در انجام واکنش نداشته اند. به چنین یون هایی که عیناً در دو طرف واکنش تکرار می شوند و هیچ پیوند شیمیایی جدیدی ایجاد نمی کنند یون ناظر یا تماشاگر گفته می شود. حال اگر یون های ناظر را از دو طرف حذف کنیم، آنچه که باقی می ماند به صورت زیر است:
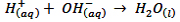
آرنیوس این و اکنش را به عنوان واکنش اصلی خنثی شدن اسید – باز در نظر گرفت.
همان طور که قبلاً گفته شد، H(aq)+ به صورت آزاد نمی تواند وجود داشته باشد چون جذب آب شده و تبدیل به یون هیدرونیم (H3Oaq+) می شود، امُا در زمان آرنیوس هنوز یون هیدرونیم کشف نشده بود. به هر حال امروزه واکنش خنثی شدن را به این صورت نشان می دهیم:
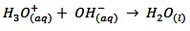
مدل آرینوس یک ایراد مهم دارد. آرنیوس اسید و باز را به محیط آبی محدود کرده بود. حال آن که گاهی یک اسید و یک باز می توانند بدون حضور آب و در فازی غیر محلول، اثر یکدیگر را خنثی کنند.
واکنش آمونیاک با هدروژن کلرید که منجر به تولید نمکی به نام آمونیوم کلرید یا نشادر می شود، بیان گر محدودیت مدل آرنیوس است.
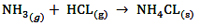
آمونیوم کلرید یا نشادر (NH4CL) یک جامد یونی سفید رنگ است امّا در لحظه ی تشکیل در این واکنش به صورت ریز ذره های معلّق در هوا است که به شکل یک ابر سفید رنگ دیده می شوند. این ذرات بعد از مدتی ته نشین شده و پودر سفید رنگ NH4CL به دست می آید.

سوال: کدام عبارت در ارتباط با مدل آرنیوس نادرست است؟
1- تنها در حالت محلول قابل استفاده است.
2- تعریف محدودی از اسید و باز ارائه می کند.
3- باز آرنیوس ماده ای است که در حلال معین حل می شود و OH(aq)- را تولید یا آزاد می کند.
4- آرنیوس این مدل را با پژوهش روی برقکافت ترکیب های محلول در آب ارائه داد.
دبیرستان شهید نصیری
محمدمهدی یوسفی
استاد راهنما: اقای سلامی
موضوع: مدل های ارنیوس
چهارم تجربی
ساس:93-94
مدل ار نیوس

در دهه ی 1890 یک شیمی دان سوئدی به نام سوانت آرنیوس طی پژوهش هایی روی رسانایی الکتریکی و برقکافت ترکیب های محلول در آب، به مدلی برای اسیدها و بازها دست یافت. در این مطلب به تشریح این مدل تحت عنوان مدل
آرنیوس خواهیم پرداخت.
اسید آرنیوس:
ماده ای است که در آب حل می شود و یون هیدروژن(H(aq)+) تولید یا آزاد می کند.
![]()
چکیده: تمام فرآیندهای برگشت پذیر ، تمایل رسیدن به یک حالت تعادلی را دارند. برای یک واکنش برگشت پذیر ، حالت تعادل وقتی برقرار میشود که سرعت واکنش رفت برابر با سرعت برگشت باشد. در یک واکنش تعادلی ، از تقسیم ثابت سرعت واکنش رفت Kf بر ثابت واکنش برگشت ، Kr ، ثابت دیگری بدست میآید که ثابت تعادل شیمیایی ، K ، نامیده میشود.
این یک انیمیشن درباره ی اصل لوشاتلیه
البته اگه انگلیسی حالیت میشه برو
http://www.mhhe.com/physsci/chemistry/essentialchemistry/flash/lechv17.swf
اسیدها موادی ترش مزهاند که خاصیت خورندگی دارند و شناساگرها را تغییر رنگ میدهند و بازها را خنثی میکنند. بازها موادی با مزه گس هستند که تلخ اند و حالتی مانند صابون در تماس با دست دارند، شناساگرها را تغییر رنگ میدهند و اسیدها را خنثی میکنند. همچنین اگر یک اسید و یک باز با هم واکنش بدهند تولید نمک و گاز هیدروژن می کنند.
قسمت 1 :
الکتروشیمی و واکنشهای اکسایش-کاهش
دبیرستان شهید نصیری
محمد مهدی یوسفی
استاد راهنما :اقای سلامی
چهارم تجربی
موضوع: نظریه برخورد
مقدمه
چون قوانین بقا در مکانیک کوانتومینیز معتبر هستند، لذا نتایجی که از استعمال آنها حاصل میشود که در مورد ذراتی با اندازههای اتمی و زیراتمی و کلان نیز معتبر است. در بیشتر مسائل برخورد ، ذرات برخورد کننده با سرعت ثابت حرکت میکنند و مدتی قبل از برخورد و بعد از آن تحت تأثیر هیچگونه نیرویی قرار نمیگیرند، در حالی که به هنگام برخورد ، تحت تأثیر نیروهایی هستند که بر یکدیگر وارد میکنند.
بنابراین از آنچه گفته شد، میتوان نتیجه گرفت که برخورد را میتوان با توجه به نوع و اندازه ذرات برخورد کننده مورد مطالعه قرار داد. به عنوان مثال ، در برخورد دو ذره با اندازههای بزرگ ، برخورد و تماس ذرات با یکدیگر کاملا اتفاق میافتد، در صورتی که در برخورد ذرات باردار اصلا تماسی بین ذرات صورت نمیگیرد، بلکه ذرات در اثر نیروهایی که به یکدیگر وارد میکنند، از کنار یکدیگر پراکنده میشوند. بنابراین ، در حالت کلی برخورد را میتوان از دو دیدگاه مکانیک کلاسیکو مکانیک کوانتومی مورد مطالعه قرار داد.
دیبرستان شهید نصیری
محمد مهدی یوسفی
استاد راهنما:اقای سلامی
موضوع :سینتیک شیمیایی
چهارم تجربی
سال:93-94
سینتیک شیمیایی
چکیده: در حالت کلی سینتیک شیمیایی را میتوان علم مطالعه سیستم های ناظر برتجزیه شیمیایی و یا تغییر حالت مولکول ها دانست. به عبارت دیگر سینتیک را میتوان علم مکمل ترمودینامیک دانسته و سیستم هایی را که توزیع انرژی آنها با زمان تغییر مینماید مطالعه کرد. نظریههایی که اثرات متقابل شیمیایی را توجیه میکنند بطور گستردهای بر اساس نتایج تجربی پایه گذاری شدهاند که با روشهای ترمودینامیکی و سینتیکی به دست میآیند.
متن مقاله:
محمد مهدی یوسفی
چهارم تجربی
استاد راهنما: اقای سلامی
موضوع :تعادل شیمیایی
سال : 93-94
تعادل شیمیایی، معرفی واکنش ها و سامانه های تعادلی
این مقاله سرفصلی برای شروع مبحث آشنایی با تعادل های شیمیایی است. در این جا ابتدا شما را با واکنش های برگشت پذیر که مبنای درک عنوان این بخش یعنی تعادل شیمیایی است، آشنا می کنیم و به دنبال آن ویژگی های عمومی سامانه های تعادلی را برخواهیم شمرد.