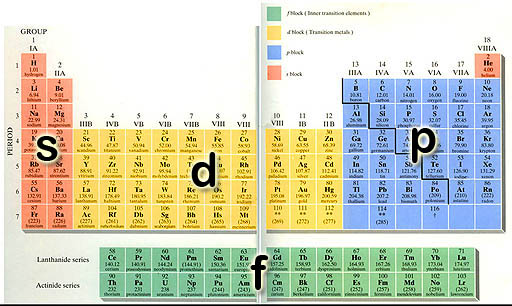
معرفی گروه چهاردهم: گروه کربن یکی ازگروه هایجدول تناوبی عناصر است کهشامل کربن(C), سیلیسیوم (Si), ژرمانیوم(Ge), قلع(Sn), سرب(Pb)، و آن ان کوادیوم(Uuq) است.......
معرفی کربن:
- کربن عنصری شیمیائی درجدول تناوبی است، با نشان C و عدد اتمی ۶. کربن عنصری غیر فلزی و فراوان، چهارظرفیتی ودارای سه آلوتروپ میباشد:
- الماس (سختترین کانی شناخته شده)
- گرافیت(یکی از نرمترین مواد)
- Covalend bound sp1 orbitals are of chemical interest only
فولریت (فولرین ها، مولکولهایی در حد بیلیونیوم متر هستند که در شکل ساده آن، ۶۰ اتم کربن یک لایه گرافیتی با ساختمان ۳ بعدی منحنی، شبیه به روروئک (روروئکی که قسمت جلوی آن مانند چوب اسکی خم شده)، تشکیل میدهند.
دوده چراغ از سطوح کوچک گرافیت تشکیل شده. این سطوح بصورت تصادفی توزیع شده، به همین دلیل کل ساختمان آن همسنگرد (ایزوتروپیک) است.
چنین کربنی همسانگرد و مانند شیشه محکم است. لایههای گرافیت آن مانند کتاب مرتب نشدهاند، بلکه مانند کاغذ خرد شده میباشند.
الیاف کربن شبیه کربن شیشهای میباشند. تحت مراقبتهای ویژه (کشیدن الیاف آلی و کربنی کردن) میتوان لایههای صاف کربن را در جهت الیاف مرتب کرد. هیچ لایه کربنی در جهت عمود بر محور الیاف قرار نمیگیرد. نتیجه الیافی با استحکام بیشتر از فولاد میباشد. کربن در تمامی جانداران وجود داشته و پایه [شیمی آلی] را تشکیل میدهد. همچنین این غیرفلز ویژگی جالبی دارد که میتواند با خودش و انواع زیادی ازعناصر دیگر پیوند برقرار کند(تشکیل دهنده بیش از ده میلیون ترکیب). در صورت ترکیب بااکسیژن تولید دی اکسید کربن میکند که برای رویش گیاهان، حیاتی میباشد. در صورت ترکیب با هیدروژن ترکیبات مختلفی بنام هیدروکربنها را بوجود میآورد که به شکل سوختهای فسیلی، در صنعت بسیار بنیادی هستند. وقتی هم با اکسیژن و هم باهیدروژن ترکیب گردد، گروه زیادی از ترکیبات را از جمله اسیدچرب را میسازند که برای حیات و استر، که طعم دهنده بسیاری از میوهها است، ضروری است.ایزوتوپ c14 به طور متداول در سن یابی پرتوزایشی کاربرد دارد.
معرفی سلیسیم:
سیلیسیم با نماد Si عنصری شیمیایی از خانوادهٔ شبه فلز است که در گروه چهارم و دورهٔ سوم جدول تناوبی عنصرها جای دارد.عدداتمی این عنصر ۱۴ است و چهار الکترون در لایهٔ ظرفیت دارد. جرم اتمی سیلیسیم ۲۸٫۰۸۶ است و دارای سه ایزوتوپ پایدار میباشد. واکنش پذیری این عنصر کمتر ازکربن نافلز هم گروه و بالاسری خود است ولی واکنش پذیری آن ازژرمانی شبه فلز پایین دستی اش بیشتر است. ستیز بر سر ویژگیهای سیلیسیم به روز نخست که آن را پیدا کردند باز میگردد. نخستین بار سیلیسیم در سال ۱۸۲۴ به صورت پالوده (خالص) فراوری شد. نام آن از واژهٔ لاتین silicis به معنی سنگ چخماق گرفته شدهاست و-ium که در انتهای آن گذاشته شده برای اشاره به ویژگیهای فلزی آن است، پسوندی که در بسیاری زبانهای غیر انگلیسی کاربرد دارد. البته نامی که در انگلیسی برای آن بکار میرود Silicon است که برای همانندی با دیگر نافلزها مانندکربن برگزیده شدهاست. این تغییر نام در سال ۱۸۳۱ پیشنهاد شد.
سیلیسیم از دید فراوانی برپایهٔ جرم، هشتمین عنصر فراوان در جهان است. البته به سختی می توان آن را به صورت خالص و آزاد در طبیعت پیدا کرد. سیلیسیم را بیشتر می توان درگردوغبار،ماسه، سیارک هاوسیارهها و در قالب سیلیسیم دی اکسید(سیلیس) و یاسیلیکات ها پیدا کرد. بیش از ۹۰٪ پوستهٔ زمین ازکانی سیلیکات ساخته شدهاست به همین دلیل سیلیس پس ازاکسیژن فراوان ترین ماده در پوستهٔ زمین است (نزدیک به ۲۸٪ بر پایهٔ جرم)
بیشتر سیلیسیمی که به صورت تجاری کاربرد دارد بدون هیچ گونه جداسازی مورد بهره برداری قرار میگیرد و خیلی کم بر روی ترکیب طبیعی آن فراوری صورت میگیرد. در بخش صنعت ساختمان و تولید سرامیکهم هنگام کاربرد رس، ماسه و سنگهای سیلیسی همین رویکرد وجود دارد. سیلیکاتها برای ملات واندودگچ وسیمان به سیمان پورتلند میروند و پس از آنکه باشن و ماسههای سیلیسی آمیخته شدند از آنهابتن ساخته میشود. کاربرد دیگر ماده درسرامیک برخی ابزارهای خانگی مانندپرسلان،شیشه های سنتی آهک سوددار با پایهٔ کواتز و... است. سیلیسیم کاربید از ترکیبهای امروزی تر سیلیسیم است که از آن سرامیکهای پرمقاومت ساخته میشود. پلیمرهای با پایهٔ سیلیسیم راسیلیکون مینامند.
بیشتر سیلیسیم آزاد در صنعتهای پالایش فولاد، ریخته گری آلومینیم و بسیاری صنعتهای حساس شیمی (مانندسیلیس دودی) کاربرد دارد. کمتر از ۱۰ درصد سیلیسیم در ساخت نیمه رساناها به کار میرود. این سیلیسیم که بسیار پالوده شده (درجهٔ خلوص بالا دارد) شاید مهم ترین نقش را در اقتصاد دنیا داشته باشد چون صنعت الکترونیک، ساخت تراشه های مدار و درنتیجه ساخت بیشتر رایانهها وابسته به آن است.
سیلیسیم در زیست شناسی هم عنصری بسیار مهم است هرچند که به نظر میرسد اندازههای بسیار کمی از آن در بدن جانوران مورد نیاز باشد. بسیاری از گونههای اسفنج های دریایی برای ساختار بدنشان نیازمند سیلیسیم اند همچنین سیلیسیم وسیلیسیکاسید در سوخت و ساز بدن گیاهان بویژه بسیاری از علفها نقشی حیاتی دارند.
معرفی ژرمانیم:
ژرمانیومسی و دومین عنصر جدول تناوبی است. ژرمانیوم یکی از اعضای مهم خانواده نیمه رساناها میباشد و در صنعت نیمههادی کاربرد فراوان دارد. نام این عنصر لاتین واژه ژرمن (آلمان) است.
معرفی قلع:
قلع (به فارسی «اَرزيز») عنصری است شیمیایی با علامت اختصاری Sn و با شماره ۵۰ در جدول اتمی. این فلز نقرهای رنگ خاصیت چکش خواری خوبی دارد و به سادگی اکسید نمیشود و در برابرخوردگی مقاوم است. قلع در بسیاری از آلیاژها مورد استفاده قرار میگیرد.
مقاومت خوب این فلز نسبت به زنگزدگی و فرسایش باعث شده تا از آن به عنوان روکشی برای فلزات دیگر برای جلوگیری از زنگزدگی استفاده شود، از جمله قلعاندود کردن ظروف مسی و به خاطر جلوگیری از زنگ زدن مس و ورود اکسید سمی مس در غذا از قدیم الایام رواج داشتهاست. برنز نخستین آلیاژ قلع است که حدود ۵ هزار سال پیش از ترکیب مس و قلع ساخته شد و آغازگر دورانی به نام عصربرنز در تاریخ بشر شد.مسوار یکی از آلیاژهای قلع است که از عصر برنز تا قرن بیستم برای ساخت ظروف و صفحات تخت و مسطح از آن استفاده میشد. قلع بیش از ۸۵ درصد حجم مسوار را تشکیل داده و بقیه از مس، سرب یا سرمهتشکیل میشود. یکی از آلیاژهای دیگر قلع که به عنوان لحیم استفاده میشود از ترکیب بیش از ۶۰ درصد قلع و بقیه سرب تشکیل میشود. همچنین بخش عمدهای از مصرف قلع نیز برای روکش کردن فولاد به منظور جلوگیری از زنگ زدن است. سمیت پائین قلع باعث میشود تا ظروف فلزی با روکش قلع برای نگهداری مواد غذایی استفاده فراوانی داشته باشند.
قلع فلزی است چکش خوار، قابل انعطاف، شدیدا" بلورین وسفید نقرهای که ساختار بلوری آن هنگام خم شدن قطعهای از قلع صدای خاصی ایجاد میکند( علت آن شکست بلورها است).این فلز دربرابر فرسایش ناشی از آب تقطیر شده دریا و آب لوله کشی مقاومت میکند اما بوسیله اسیدهای قوی و موادقلیایی و نمکهای اسیدی مورد حمله قرار میگیرد. هنگامیکه اکسیژن بصورت محلول است قلع بعنوان کاتالیزور عمل کرده و واکنشهای شیمیایی را تسریع میکند. درصورتیکه آنرا درحضور آزمایشهای مربوط به هوا حرارت دهند Sn۲ حاصل میشود. Sn۲ اسید ضعیفی بوده و با اکسیدهای بازی تولید نمکهای قلع میکند.قلع را میتوان به مقدار زیادی جلا داد و بعنوان پوشش سایر مواد جهت ممانعت از فرسودگی یا واکنشهای شیمیایی دیگرمورد استفاده قرار میگیرد.این فلز مستقیما" با کلر و اکسیژن ترکیب میشود و و جایگزین هیدروژن اسیدهای رقیق میگردد.قلع در دماهای معمولی انعطاف پذیر است اما در صورتیکه گرم شود شکننده میشود.
معرفی سرب:
سرباز عنصرهای شیمیاییواسطه درجدول تناوبی است. سرب همچنین در رده فلزها قرار دارد. این فلز تشعشعات هستهای را عبور نمیدهد. سرب در طبیعت به شکل کانی به نام گالن (سیستم تبلور کوبیک یا مکعبی) یافت میگردد.
سرب عنصر شیمیایی است که در جدول تناوبی با نشان Pb و عدد اتمی ۸۲ وجود دارد. سرب عنصری سنگین، سمی و چکش خوار است که دارای رنگ خاکستری کدری میباشد. هنگامیکه تازه تراشیده شده سفید مایل به آبی است اما در معرض هوا به رنگ خاکستری تیره تبدیل میشود. از سرب در سازههای ساختمانی،خازنهای اسید سرب، ساچمه و گلوله استفاده شده و نیز بخشی از آلیاژهای لحیم، پیوتر وآلیاژهایگدازپذیر میباشد. سرب سنگینترین عنصرپایدار است.
سرب فلزی است براق، انعطاف پذیر، بسیار نرم، شدیداً چکش خوار و به رنگ سفید مایل به آبی که از خاصیت هدایت الکتریکیپایینی برخوردار میباشد. این فلز حقیقی به شدت در برابر پوسیدگی مقاومت میکند و به همین علت از آن برای نگهداری مایعات فرسایشگر (مثل اسید سولفوریک) استفاده میشود. با افزودن مقادیر خیلی کمی آنتیموان یا فلزات دیگر به سرب میتوان آنرا سخت نمود.
| گروه→ | ۱۴ |
|---|---|
| ↓ دوره | |
| ۲ | 6 C |
| ۳ | 14 Si |
| ۴ | 32 Ge |
| ۵ | 50 Sn |
| ۶ | 82 Pb |
| ۷ | 114 Uuq |


 فرمول نویسی فقط در یک صفحه A4
فرمول نویسی فقط در یک صفحه A4  جزوه شیمی 2
جزوه شیمی 2