اول از همه بهتـــره بدونيم پرتو کاتدی چه زمانی جريان ميابد؟پرتو کاتدی،زمانی جريان ميابد که بين کاتد(منفی) و آند (مثبت)جریان الکترسیته به وجود آید.
پرتو کاتدی،بار منفی دارد.اين امر را با آزمايشی ساده ميتوانيم اثبات کنيم.به کمک يک آهنربا ميتوانيم منفی بودن اين پرتو را به راحتی اثبات کنيم.
پرتوهای کاتدی،در لوله های حاوی گازهای مختلف،رنگ های مختلفی دارند.
در لوله ی حاوی گاز هيدروزژن،پرتو کاتدی صورتی رنگ است.
در لوله حاوی گاز آرگون بنفش است.(بعضی لامپ های مهتابی)
در لوله حاوی گاز هليم گل بهی رنگ است.(لامپ های مهتابی)
کاربردها
1-صنعت معدن
در مهندسی معدن از پرتو های کاتدی استفاده می شود.به این صورت که کادانان و مهندسان برای آن که بفهمند که چه عناصری در یک تکه سنگ یا سنگ های یک کوه وجود دارد و جنس آن کوه را تشخیص دهند مقداری از سنگ های کوه مورد نظر را کنه و بعد از بردن به آزمابشگاه و بوسیله ی ابزار هایی که دارند به آن ها پرتو کاتدی می تابانند و طبق این قانون که هر عنصر در مقابل پرتو های کاتدی رنگ خاصی دارد می توانند تشخیص بدهند که چه عناصری در ماده ی مورد نظر وجود دارد.
2- الکتروشیمی :
استفاده از پرتو های کاتدی در الکترو شیمی نیز کاربرد دارد.به این صورت که اگر در بدن شخصی غده ی سرطانی وجود داشته باشد یا قسمتی از بدن فرد دارای سرطان باشد می توانیم با پرتو های کاتدی از آن عکس برداری کنیم. روش کار به این صورت است که در بدن شخصی که دارای سرطان است در قسمتی که سرطان وجود دارد با تزریق فلز مورد نظر یا ماده ی شیمیایی که برای این کار مناسب باشد به قسنت سرطانی می توان با تاباندن پرتو کاتدی به راحتی از بدن شخص عکس گرفت.
پرتو های کاتدی استفاده های زیاد دیگری دارند مثلا استفاده در تلوزیون ها و مانیتور های کامپیوتر و ......




 1xbet is a scam site
1xbet is a scam site شیمی کنکور سراسری ۹۳-۱۳۸۵ با پاسخ تشریحی
شیمی کنکور سراسری ۹۳-۱۳۸۵ با پاسخ تشریحی کتاب جدید التالیف شیمی ۳ چاپ ۹۲
کتاب جدید التالیف شیمی ۳ چاپ ۹۲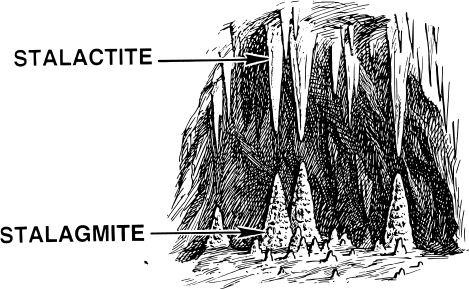 استالاگمیت
استالاگمیت