خواص آب
آب یکی از مواد مایع و فراوانترین مادهٔ مرکب بر روی سطح کره زمین و بستر اولیه حیات به شکلی که امروزه میشناسیم، است. بیش از ۷۵٪ وزن یک انسان از آب تشکیل شدهاست و نیز بیش از ۷۰٪ سطح کره زمین را آب پوشانده است (نزدیک به ۳۶۰ میلیون از ۵۱۰ میلیون کیلومتر مربع) با وجود این حجم عظیم آب تنها ۲ درصد از آبهای کره زمین شیرین و قابل شرب است و باقی آن به علت محلول بودن انواع نمکها خصوصاً نمک طعام غیر قابل استفاده است. از همین دو درصد آب شیرین بیش از ۹۰ درصد به صورت منجمد در دو قطب زمین و دور از دسترس بشر واقع شدهاست.
نامگذاری آب
آب در گویشهای محلی به نامهای مختلف یاد میشود. برای مثال در زبان خراسان جنوبی به آن ِأو(به ضم همزه)(ow)می گویند.؛ در فیزیک بر اساس حالت ماده آب معمولاً به این نامها خوانده میشود:
ویژگیهای فیزیکی و شیمیایی
مولکول آب
فرمول شیمیایی آب، H۲O است؛ مولکول آب از دو اتم هیدروژن و یک اتم اکسیژن تشکیل شدهاست که با پیوندهای کووالانس به هم متصل شدهاند. اتمهای هیدروژن دارای بار مثبت هستند و با زاویه نزدیک به ۱۰۵ درجه در اطراف اتم اکسیژن قرار گرفتهاند که این موضوع باعث قطبی شدن پیوندهای مولکول آب شدهاست. جرم مولی آب برابر ۱۸ گرم بر مول میباشد.
خواص فیزیکی آب
بیبو، بیرنگ و بیطعم. آب خواص ویژهای دارد که آن را از دیگر مایعات متمایز کردهاست. از این خواص ویژه میتوان به ظرفیت گرمایی بالا، افزایش غیرعادی حجم به هنگام انجماد، کشش سطحی بالا، گرانروی بسیار پایین و بالا بودن گرمای نهان تغییر فاز اشاره نمود. دلیل بسیاری از این خاصیتها وجود پیوند هیدروژنی در میان مولکولهای آب است. چگالی آب
در دمای ۲۵ درجه سانتیگراد و فشار ۱ آتمسفر برابر ۰.۹۹۸ گرم بر سانتمیتر مکعب است. آب در فشار ۱ آتمسفر در دمای ۱۰۰ درجه سانتیگراد میجوشد و در دمای صفر درجه سانتیگراد منجمد میشود. همچنین آب در ۴ درجه سانتی گراد بیشترین چگالی یعنی ۱ گرم بر سانتیمتر مکعب را دارد، که این مسئله از لحاظ علمی بسیار جالب است و یک استثنا به شمار میآید.
خواص شیمیایی آب
آب از نظر شیمیایی از ترکیب دو اتم هیدروژن با یک اتم اکسیژن به دست میآید. قدرت حلالیت بسیار بالایی داشته و عملاً پرکاربردترین حلّال در صنعت و فرایندهای شیمیایی است. بسیاری از فرایندهای شیمیایی و بیوشیمیایی در محیط آبی با سرعتی به مراتب بیش از هر محیط دیگری انجام میگیرد. این ماده در برابر دمای بالا مقاومت نشان داده و تا دمای بیش از ۱۰۰۰ درجه سانتیگراد نیز تجزیه نمیشود. برای تجزیهٔ آب بهترین راه بهره گیری از فرایند الکترولیز در دستگاهی به نام ولتامتر است. به این صورت که با استفاده از دو الکترود (بهترین جنس برای این منظور پلاتین است) جریان برق مستقیم را از آب عبور دهیم. به این ترتیب در قطب مثبت اکسیژن و در قطب منفی هیدروژن آزاد خواهد شد.
منـابع:
1. وب سایت ویکی پدیا فارسی
2. وب سایت تبیان
3. وب سایت دانشنامه رشد
تهیّه کننـده : امیر احمدی ، دبیرستان شهید نصیری ، کلاس 05


 فرمول نویسی فقط در یک صفحه A4
فرمول نویسی فقط در یک صفحه A4 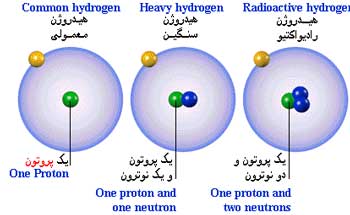 ایزوتوپ - سعید رفیع زاده
ایزوتوپ - سعید رفیع زاده قابل توجه دانش آموزان سوم تجربی دبیرستان شهید نصیری
قابل توجه دانش آموزان سوم تجربی دبیرستان شهید نصیری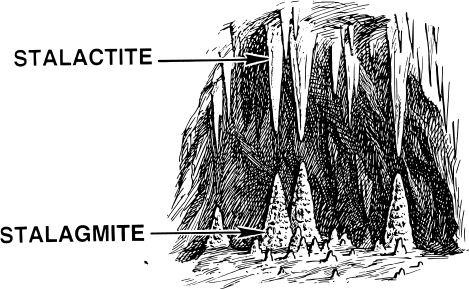 استالاگمیت
استالاگمیت